Лабораторная работа: Тепловые эффекты химических реакций
Равновесные парциальные давления определим по закону Дальтона:
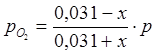 ;
;
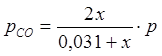 ;
;
где ![]() - общее давление. Закон действующих масс для данной реакции запишется так:
- общее давление. Закон действующих масс для данной реакции запишется так:
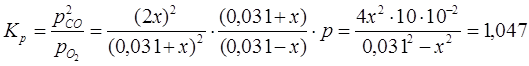
![]()
С учетом того, что углерода расходуется в 2 раза больше, чем кислорода, то количество прореагировавшего углерода составит 0,005 молей.
4) Определение изменения энергии Гиббса для начала реакции
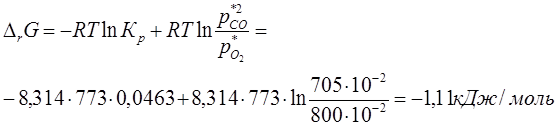
Самостоятельная работа № 5
Вариант 8
Зависимость константы равновесия реакции от температуры (табл. 9) выражается уравнением ![]() коэффициенты a, b, c и d приведены в табл. 1, давление выражено в Паскалях:
коэффициенты a, b, c и d приведены в табл. 1, давление выражено в Паскалях:
1. определите константу равновесия реакции при Т, К;
2. постройте график зависимости ![]() в интервале температур от (Т – 100) до (Т + 100) К;
в интервале температур от (Т – 100) до (Т + 100) К;
3. укажите, как изменяется константа равновесия при повышении температуры;
4. определите тепловой эффект реакции ![]() при Т, К;
при Т, К;
5. сопоставьте тепловой эффект, вычисленный в п. 4, с тепловым эффектом, вычисленным по закону Кирхгофа при температуре Т, К;
6. определите стандартное сродство реагирующих веществ при температуре Т, К.
|
Реакция (А) |
К |
Т, К |
|
|
|
500 |
Таблица 1
|
a |
b |
c |
d |
|
– 4600 |
0,623 |
К-во Просмотров: 858
Бесплатно скачать Лабораторная работа: Тепловые эффекты химических реакций
|