Реферат: Бионеорганическая химия
![]() Другой тип биополимерных лигандов - белки (протеины). Белки представляют собой полимерные образования, в которых в том или ином порядке чередуются 23 α-аминокислоты. Строение всех аминокислот может быть описано формулой
Другой тип биополимерных лигандов - белки (протеины). Белки представляют собой полимерные образования, в которых в том или ином порядке чередуются 23 α-аминокислоты. Строение всех аминокислот может быть описано формулой
Различаются они только природой радикала R. α-Аминокислоты, вступая в реакцию полимеризации, образуют пептидную цепь:
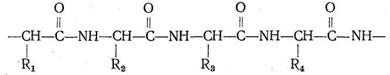
Подобно тому как из 32 букв алфавита путем их различного сочетания можно составить огромное количество слов, так из 23 α-аминокислот посредством их сочленения в том или ином порядке получается все многообразие белковых тел, существующих в природе, образуется так называемая первичная белковая структура. Кроме того, рассматривают вторичную, третичную и четвертичную структуру.
Вторичная структура (α - и β-конформации) возникает в результате взаимодействия полипептидных цепей друг с другом. α-Конформация имеет спиралеобразное строение, каждый виток спирали содержит от трех до семи аминокислотных фрагментов. Взаимодействие между соседними полипептидными цепями в такой спирали осуществляется посредством водородных связей, образованных карбонильным кислородом одной цепи с иминогруппой другой цепи:
![]()
Редко встречающаяся β-конформация содержит вытянутые друг возле друга неспиральные полипептидные цепи.
Третичная структура белка - это глобулы, образованные α-вторичной структурой в результате свертывания полипептидных цепей в клубки. Свертывание α-спиралей в глобулы происходит в результате взаимодействия друг с другом гидрофобных участков спирали, электростатического взаимодействия заряженных участков цепи, образования сульфидных мостиков и водородных связей.
Четвертичная структура возникает в результате объединения глобул в еще более сложную структуру.
Свойства белков как биолигандов определяются содержанием в полипептидных цепях донорных атомов азота и кислорода, которые могут участвовать в образовании хелатных циклов и макроциклических комплексов. Кроме того, к полипептидным цепям через различные функциональные группы могут быть привязаны порфириновые кольца. Порфирин содержит четыре пиррольных ядра (с различными заместителями):
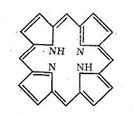
Как видно из схемы, порфирин представляет собой пример макро-циклического лиганда с четырьмя донорными атомами азота, которые координируются ионами металла, если создаются условия для вытеснения двух протонов порфирина и замещения их на ионы металла. Размер полости порфирина составляет около 2Ǻ (диаметр). Порфирин принадлежит к числу «жестких» лигандов, структура которых (и размер полости) мало зависит от природы координируемого иона металла. Порфириновые металлоциклы содержатся в хлорофилле и гемоглобине. Строение порфиринсодержащих комплексов биометаллов будет рассмотрено дальше.
Нуклеиновые кислоты - третий вид наиболее важных биополимерных лигандов. Роль нуклеиновых кислот в биосистемах состоит в хранении и передаче информации о строении синтезируемых организмом белков. Нуклеиновые кислоты состоят из мономеров - нуклеотидов. Каждый нуклеотид содержит фрагменты углевода, гетероциклического основания и остаток фосфорной кислоты. Нуклеотиды соединяются в нуклеиновые кислоты по следующей схеме:
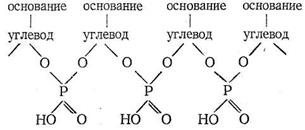
Примером гетероциклических оснований могут служить аденин и урацил:

В качестве углеводного компонента нуклеиновых кислот выступают рибоза и продукт ее восстановления - дезоксирибоза:
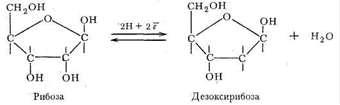
В зависимости от природы углеводного фрагмента нуклеиновые кислоты делятся на две группы: рибонуклеиновые (РНК) и дезоксирибонуклеиновые (ДНК) кислоты. ДНК в растворах имеют строение двойных спиралей. Внутрь спирали обращены гетероциклические основания, скрепленные друг с другом водородными связями, наружу обращены фосфатные группировки. Совершенно ясно, что ДНК и РНК обладают свойствами лигандов: донорные атомы имеются во всех фрагментах нуклеиновых кислот.
Кроме белков, полисахаридов и нуклеиновых кислот в биосистемах обычно присутствует большое число других химических соединений, проявляющих свойства лигандов и обладающих биологической активностью. Среди них особенно важную роль играют различные органические кислоты, как насыщенные, так и ненасыщенные, например аскорбиновая кислота:
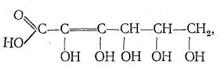
производные фосфорной кислоты (такие, как аденозинфосфаты, липиды) и др.
3 . Биологическая роль неорганических соединений
Биологическая роль неорганических веществ (О2 , СО2 , N2 и т. д.), а также ионов металлов и соединений, включающих эти ионы и атомы металлов, связанные ковалентно, чрезвычайно важна и многообразна. Один из основных процессов, связанных с участием неорганических соединений, - процесс фотосинтеза. Именно взаимодействие Н2 О и СО2 - двух неорганических соединений - приводит (при катализирующем действии хлорофилла - магниевого комплекса порфирина) к синтезу крахмала С6Н12О6 с выделением кислорода:
![]()
Эта реакция проходит через большое число стадий, но суть фотосинтеза состоит все же в соединении неорганических веществ в углевод. Углеводы, синтезируемые в растениях, потребляются травоядными животными. В результате пищеварения и дальнейших сложных превращений в организме травоядных образуются белки и жиры, служащие пищей для хищников и всеядных животных. К числу последних может быть отнесен и человек. Источником энергии, необходимой для жизнедеятельности человека и животных, являются белки, жиры и углеводы, содержащиеся в продуктах питания растительного и животного происхождения. Окисляясь (неорганическим) молекулярным кислородом, эти вещества, вернее продукты их деструкции, дают организму энергию, затрачиваемую на другие жизненно важные химические процессы и превращаемую в механическую энергию (движение), электрическую энергию и др.
Уже упоминалось, что важнейшую роль в процессах метаболизма играют ионофоры, регулирующие содержание акваионов щелочных и щелочноземельных металлов во внеклеточном и внутриклеточном пространстве, а также ферменты. Ферменты - всегда белковые вещества. Они ускоряют или ингибируют важнейшие процессы в организме, способствуют переносу в тканях кислорода и углекислого газа, переносу электронов, ускорению гидролитических процессов.
Роль акваионов металлов и металлсодержащих комплексов в живых организмах состоит в регуляции процессов, связанных с получением, преобразованием и распределением в организме энергии, выделением вредных для организма продуктов реакции.
Рассмотрим на ряде примеров биологическую роль акваионов металлов и их комплексов с биолигандами.
Транспорт ионов металлов и других неорганических компонентов в растительных и животных организмах