Реферат: Главные элементы жизни: азот и фосфор
С водородом азот соединяется в присутствии катализатора при высоком давлении и температур
![]()
![]()
![]() N2 + 3H3 2NH3
N2 + 3H3 2NH3
При температуре электрической дуги (3000-4000о С) азот соединяется с кислородом:
![]()
![]() N2 + O2 2NO
N2 + O2 2NO
Азот образует с водородом несколько прочных соединений, из которых важнейшим является аммиак. Электронная формула молекулы аммиака такова:
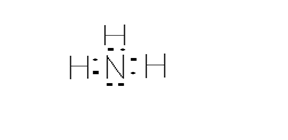
![]() Получение и применение аммиака. В лабораторных условиях аммиак обычно получают слабым нагреванием смеси хлорида аммония с гашеной известью:
Получение и применение аммиака. В лабораторных условиях аммиак обычно получают слабым нагреванием смеси хлорида аммония с гашеной известью:
2NH4 Cl + Ca (OH)2 = CaCl2 + 2NH3 + 2H2 O
Основным промышленным способом получения аммиака является синтез его из азота и водорода. Реакция экзотермичная и обратимая:
![]()
![]() N2 + 3H2 2NH3 + 92кДж
N2 + 3H2 2NH3 + 92кДж
Она протекает только в присутствии катализатора Губчатого железа с добавками активаторов - оксидов алюминия, калия, кальция, кремния (иногда и магния)
Физические свойства аммиака. Аммиак – бесцветный газ с характерным резким запахом, почти в два раза легче воздуха. При увеличении давления или охлаждении он легко сжимается в бесцветную жидкость. Аммиак хорошо растворим в воде. Раствор аммиака в воде называется аммиачной водой или нашатырным спиртом. При кипячении растворённый аммиак улетучивается из раствора.
Химические свойства аммиака. Большая растворимость аммиака в воде обусловлена образованием водородных связей между их молекулами. Гидроксид – ионы обуславливают слабощелочную (их мало) реакцию аммиачной воды. При взаимодействии гидроксид - ионов с ионами NH4 + снова образуются молекулы NH3 и H2 O, соединённые водородной связью, т. е. реакция протекает в обратном направлении. Образование ионов аммония и гидроксид – ионов в аммиачной воде можно выразить уравнением.
![]()
![]()
![]()
![]() NH3 + H2 O NH3 . H2 ONH4 + + OH—
NH3 + H2 O NH3 . H2 ONH4 + + OH—
В аммиачной воде наибольшая часть аммиака содержится в виде молекул NH3 , равновесие смещено в сторону образования аммиака, поэтому она пахнет аммиаком. Тем не менее водный раствор аммиака по традиции обозначают формулой NH4 OH и называют гидроксидом аммония, а щелочную реакцию раствора аммиака объясняют как результат диссоциации молекул NH4 OH:
![]()
![]() NH4 OH NH4 + + OH—
NH4 OH NH4 + + OH—
А так как в растворе аммиака в воде концентрация гидроксид – ионов невелика, то гидроксид аммония относится к слабым основаниям.
Аммиак сгорает в кислороде и в воздухе (предварительно подогретом) с образованием азота и воды:
4NH3 + 3O2 = 2N2 + 6H2 O
В присутствии катализатора [например, оксида хрома (III )] реакция протекает с образованием оксида азота (II) и воды:
Cr2 O3
4NH3 + 5O2 = 4NO + 6H2 O
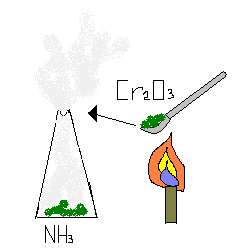
Аммиак взаимодействует с галогенами, при этом выделяется азот и водородное соединение галогена:
2NH3 + 3Br2 = 6HBr + N2
2NH3 + 3Cl2 = 6HCl + N2
Аммиак – сильный восстановитель. При нагревании он восстанавливает оксид меди (II), а сам окисляется до свободного азота:
3Cu+2 O + 2N—3 H3 = 3Cu0 + N2 0 + 3H2 O
2N—3 – 6e = N2 1