Реферат: Кинетика двухатомного газа
Займемся вычислением свободной вращательной энергии. Если температура настолько высока, что
(«вращательный квант» ћ²/2I мал по сравнению с T)1 ), то в сумме (3) основную роль играют члены с большими К. Но при больших значениях К вращение молекулы квазиклассично. Поэтому в этом случае статистическая сумма Zвр может быть заменена соответствующим классическим интегралом:
(9)
где ε(М)—классическое выражение кинетической энергии вращения как функции момента вращения М. Вводя связанную с молекулой вращающуюся систему координат ξ, η, ζ, с осью ζ, вдоль оси молекулы и, имея в виду то, что двухатомная молекула обладает двумя вращательными степенями свободы, а момент вращения линейной механической системы перпендикулярен к ее оси, пишем:
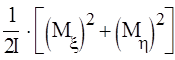 |
ε(M)= (10)
Элемент dτ вр есть деленное на (2лћ)2 произведение дифференциалов dM ξ dM η и дифференциалов соответствующих M ξ иM η «обобщенных координат», т. е. бесконечно малых углов поворота вокруг осей
ξ и η: d φξd φη1 ).Но произведение двух бесконечно малых углов поворота вокруг осей ξ и η есть не что иное, как элемент телесного угла d 0 ζ для направления третьей оси ζ; интегрирование по телесному углу даст 4π. Таким образом, имеем 2 ):
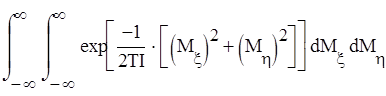 |
Zвр=4π/(2πћ)² =
=2IT/ћ²
Отсюда свободная энергия
Fвр =-NT lnT-NT ln2I/ћ² (10)
Таким образом, при рассматриваемых не слишком низких температурах вращательная часть теплоемкости оказывается постоянной и равной C вр=1 в соответствии с общими результатами классического рассмотрения идеального газа (по ½ на каждую вращательную степень свободы).Вращательная часть химической постоянной равна ξвр=ln(2I/ћ²). Мы увидим ниже, что существует значительная область температур, в которой выполнено условие T>>ћ²/2I и в то же время колебательная часть свободной энергии, а с нею и колебательная часть теплоемкости отсутствуют. В этой области теплоемкость двухатомного газа равна Cν=Cпос+Cвр, т.е.
Cν=5/2, Сp=7/2, (11)
а химическая постоянная ξ= ξпос+ ξвр:
![]()
(12)
В обратном предельном случае низких температур
T<<ћ²/2I
достаточно сохранить два первых члена суммы:
Zвр=1+3exp(-ћ²/IT),
и для свободной энергии получим в том же приближении:
Fвр=-3NTexp(-ћ²/IT). (13)
Отсюдаэнтропия
Sвр=3N ћ²/(IT)[exp(-ћ²/IT)](1+ IT/ ћ²) (14)
и теплоемкость
Свр=3N(ћ²/IT) ² exp(-ћ²/IT). (15)
![]()
Таким образом, вращательные энтропия и теплоемкость газа при T→0 обращаются в нуль в основном по экспоненциальному закону. При низких температурах,
Следовательно, двухатомный
 газ ведет себя как одноатомный; Cвр как его теплоемкость, так и химическая постоянная имеют те же значения, которые имел бы одноатомный газ с части- цами массы m.
газ ведет себя как одноатомный; Cвр как его теплоемкость, так и химическая постоянная имеют те же значения, которые имел бы одноатомный газ с части- цами массы m.
В общем случае произвольных 2IT/ ћ²