Реферат: Корпускулярно-хвильовий дуалізм речовини
Розглянемо дифракцію електронів на одній щілині. Нехай пучок електронів із швидкістю летить в напрямі осіOY так, як це показано на рис. 1.4.
Екран АВ із щілиною шириною d розміщено перпендикулярно до пучка. На другому екраніСД одержано розподіл інтенсивності, який збігається з розподілом інтенсивності при дифракції світла від однієї щілини.
На рис. 1.4 цей розподіл зображено пунктирною лінією. Максимум нульового порядку одержано з кутом дифракції , який задовольняє умову:
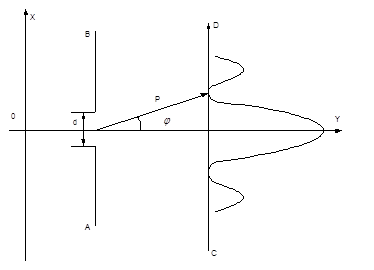
Рис. 1.4
 , (1.1.12)
, (1.1.12)
де ― довжина хвилі, яка відповідає пучку електронів.
З рис. 1.4 видно, що переважна більшість електронів формують нульовий максимум, тому вторинними максимумами в цьому випадку можна знехтувати. Якщо уявити електрони у вигляді механічних частинок, то можна стверджувати, що при їх русі із швидкістю у напрямі осі OX їх положення визначається з точністю до ширини щілини, тобто
![]() (1.1.13)
(1.1.13)
В той же час, унаслідок дифракції змінюється напрям швидкості частинок. Враховуючи лише ті електрони, які формують центральний максимум дифракції, похибку у визначенні проекції імпульсу на напрям осі OX знайдемо із умови
![]() . (1.1.14)
. (1.1.14)
З урахуванням (1.1.12) і (1.1.13) одержимо
![]() .(1.1.15)
.(1.1.15)
А оскільки не всі електрони формують центральний максимум, тому
![]() , (1.1.16)
, (1.1.16)
де x іpx ― похибки у визначені координати й імпульсу частинки;![]() – стала Планка поділена на 2
– стала Планка поділена на 2![]() .
.
Співвідношення (1.1.16) можна узагальнити для всіх напрямків, тому:
![]() ,
,
![]() , (1.1.17)
, (1.1.17)
![]() .
.
Це і є співвідношення невизначеностей Гейзенберга.
Оскільки точні значення координати й імпульсу для мікрочастинки не існують, то про траєкторію частинки в мікросвіті можна говорити лише з певним наближенням. З цієї точки зору електрони в атомі не мають точних значень електронних орбіт.
У квантовій теорії використовується також співвідношення невизначеностей для енергії Е і часуt , тобто невизначеності цих параметрів задовольняють умову:
![]() , (1.1.18)
, (1.1.18)
де E ― похибка у визначенні енергії частинки;t ― похибка у визна-ченні часу, коли частинка має енергію E .
Cпіввідношення невизначеностей неодноразово були предметом філософських дискусій. Однак вони не виражають собою певних обмежень пізнання мікросвіту, а лише указують межі використання у таких випадках понять класичної механіки.
Ще раз підкреслимо, що співвідношення невизначеностей не пов'язано з недосконалістю вимірювальної техніки, а є об'єктивною властивістю матерії: таких станів мікрочастинок, у яких і координата, і імпульс частинки мають визначене значення, просто не існує в природі.
Співвідношення невизначеностей допомагають зрозуміти багато особливостей поведінки мікрочастинок і дозволяють швидко й просто оцінити параметри їх стану. Для прикладу розглянемо застосування співвідношень невизначеностей до опису руху електрона в атомі водню.
Будемо вважати, що електрон локалізований в області простору, розміри якого дорівнюють розмірам атома. Тоді невизначеність координати електрона можна прийняти рівною радіусу атома: ∆ x = r . Звідси, відповідно до рівнянь (1.1.17), невизначеність значення імпульсу електрона ∆p =h / (2 ![]() r) . Очевидно, що значення самого імпульсу не може бути меншим його невизначеності, тому мінімально можливе значення імпульсу електрона дорівнює
r) . Очевидно, що значення самого імпульсу не може бути меншим його невизначеності, тому мінімально можливе значення імпульсу електрона дорівнює
![]() (1.1.19)
(1.1.19)
Рівняння (1.1.19) можна записати у вигляді p ∆ r = h/2π , або mvr = ћ . Цей результат – не що інше, як умова стаціонарної орбіти електрона в атомі водню відповідно до постулатів Н. Бора . Але, якщо Н. Бор увів свої постулати довільно, і тільки для атома водню, то ми одержали цю умову із загального універсального принципу – співвідношення невизначеностей.