Реферат: Ненасыщенные альдегиды и кетоны
CH3 COOH + H+ ® CH3COO+ H2 ® CH3 C+ =O ® CH2 =C=O + H+
Кетены чрезвычайно легко реагируют с водой:
CH2 =C=O + H2 O ® CH3 COOH
карбоновыми кислотами:
CH2 =C=O + CH3 COOH ® (CH3 CO)2 O.
Спиртами:
CH2 =C=O + CH3 CH2 OH ® CH3 COOCH2 CH3 .
Аминами:
CH2 =C=O + CH3 NH2 ® CH3 CONHCH3 + H2 O.
В промышленности из кетена получают уксусную кислоту, уксусный ангидрид, этилацетат, дикетен и другие вещества, являющиеся полупродуктами в производстве красителей и лекарственных веществ.
Кетен легко полимеризуется с образованием дикетена:
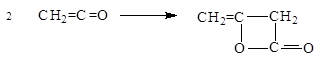 .
.
Дикетен реагирует с водой, спиртами, аминами:
CH2 =COCH2 CO + H2 O ® CH3 COCH2 COOH.
Ароматические альдегиды и кетоны
Ароматические альдегиды и кетоны характеризуются наличием карбонильной группы, связанной с углеродом бензольного ядра или боковой цепи. Альдегиды с карбонильной группой первого типа называются по соответствующим ароматическим кислотам, а с карбонильной группой в боковой цепи – как арилзамещенные альдегиды жирного ряда.
Кетоны бывают чисто ароматические (дифенилкетон или бензофенон) и жирноароматическими (метилфенилкетон или ацетофенон).
Способы получения ароматических альдегидов
Многие ароматические альдегиды могут быть получены способам, описанными для альдегидов жирного ряда (Лекция№23): окисление первичных спиртов, сухая перегонка кальциевых солей ароматической и муравьиной кислот, синтезы с участием реактивов Гриньяра и др.
1. Окисление ароматических углеводородов.
Важный способ синтеза ароматических альдегидов (в частности, бензальдегида) – окисление углеводородов кислородом воздуха на катализаторе (V2 O5 , MnO2 ):
C6 H5 -CH3 ® C6 H5 -CHO
Способ имеет как лабораторное, так и промышленное значение.
2. Формилирование ароматических углеводородов.
Для ароматического ряда известны реакции прямого введения альдегидной группы, не имеющие аналогий в жирном ряду (реакция Гаттермана-Коха):
C6 H5 CH3 + HCl+CO ® CH3 -C6 H4 -CHO
Реакция катализируется хлоридами меди и алюминия. Предполагается, что в качестве промежуточного продукта образуется хлористый формил HCOCl, не существующий в свободном виде. Бензол в эту реакцию вступает очень плохо, его гомологи дают хорошие выходы (50-60%).
3. Гидролиз гем-дигалогенпроизводных.
Существует способ получения бензальдегида через хлористый бензилиден C6 H5 CHCl2 :
C6 H5 CH3 + Cl2 ® C6 H5 CHCl2 + H2 O ® C6 H5 CHO + 2 HCl
толуол хлористый бензилиден бензальдегид