Реферат: Одно и многоатомные спирты
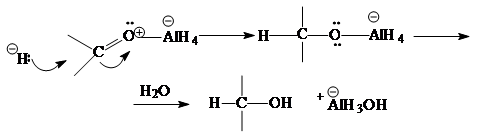
CH3 COCH3 + LiAlH4 ® (CH3 )2 -CHOH
CH3 -CHO + NaBH4 ® CH3 -CH2 -OH
Сложные эфиры также восстанавливаются алюмогидридом лития, причем оба фрагмента эфира превращаются в спирты:
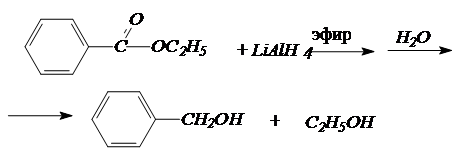
4. Синтезы спиртов с использованием реактивов Гриньяра.
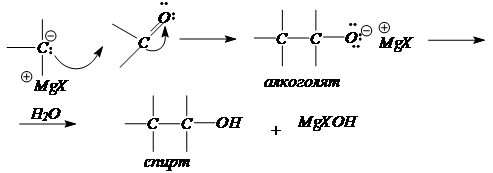
RMgHal + H2 C=O (формальдегид) ® RCH2 O - Mg+ Hal + H2 O ® R-CH2 -OH
RMgHal + R’HC=O (альдегид) ® R( R’)CHO - Mg+ Hal + H2 O ® R(R’)CH-OH
RMgHal + (R’)2 C=O (кетон) ® R( R’)2 CO - Mg+ Hal + H2 O ® R(R’)2 C-OH
По механизму это реакция нуклеофильного присоединения к карбонильной группе.
Промышленные методы получения спиртов.
1. Окисление алканов (синтез спиртов С10 -С20 ).
3 RCH2 -OH + B(OH)3 « B(OHC2 R)3 + 3 H2 O
2. Гидратация алкенов .
R-CH=CH2 + H2 O « R-CH (OH)-CH3
CH2 =CH2 + H2 O ® CH3 CH2 OH
из пропилена и н-бутилена - изопропиловый и н-бутиловый спирты:
CH3 -CH=CH2 + H2 O ® CH3 -CH (OH)-CH3
CH3 -CH2 -CH=CH2 + H2 O ® CH3 -CH2 -CH (OH)-CH3
а из изобутилена - трет-бутиловый спирт:
(CH3 )2 C=CH2 + H2 O ® (CH3 )3 C-OH
Электрофильный механизм гидратации определяет уже отмеченное выше направление присоединения (правило марковникова), а также изменение реакционной способности алкенов в ряду, определяемом сравнительной стабильностью образующихся карбокатионов:
(CH3 )2 CH=CH2 >> CH3 -CH2 -CH=CH2 > CH3 -CH=CH2 >> CH2 =CH2
3. Синтез спиртов по методу Фишера-Тропша .
СО + 2Н2 « СН3 ОН
4. Процесс оксосинтеза .
CH2 =CH2 + CO + H2 ® CH3 -CH2 -CHO
Химические свойства спиртов