Реферат: Порівняння властивостей органічних речовин
ІІІ.
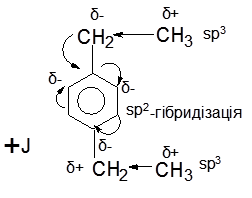
Зв'язок C-C є семіполярний, тому М=0, але дуже сильний + I
Етен,виявляючи позитивний індуктивний ефект, збільшує електронну густину бензольного ядра і поляризує його, тобто порушує в ньому рівномірний розподіл електронної густини. На вуглецевих атомах 2,4,6 виникає надлишок електронної густини
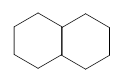
Декалін - дициклоалкан. Тому виявляє хімічні властивості циклоалканів.
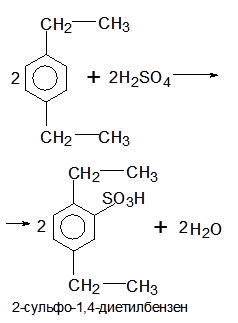
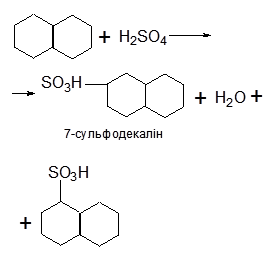
Нітрування:
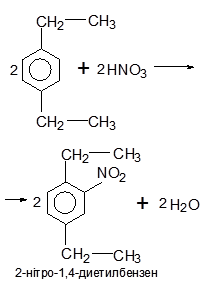
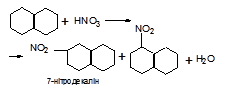
Хлорування:

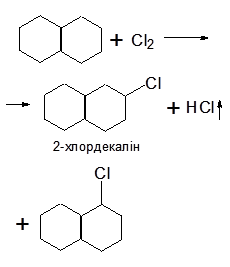
Окислення:
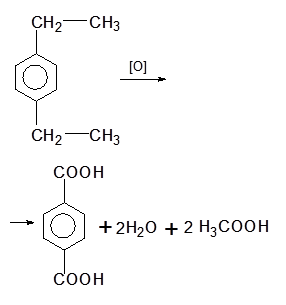

Відмінні хімічні властивості:
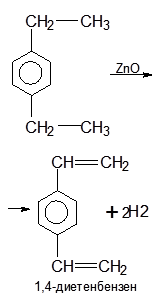
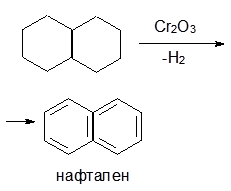
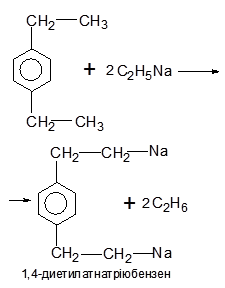
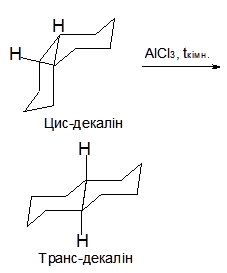
| 2-Хлорпентанол-1 і n-хлорфенол | |
|
Зв'язок між атомом вуглецю і атомом хлору ковалентний. Але хлор більш електронегативний, ніж вуглець. Тому електронна пара зв'язку С→Cl значно зміщена до атому хлору, має заряд δ+ . Отже атом хлору виявляє -J. Наявність у молекулі гідроксильної групи зумовлює кослотно-основні властивості. Оскільки атом кисню більш електронегативний, ніж атом вуглецю та водню, то електронна густина зміщується від цих атомів до кисню. Зв'язки О-Н і С-О поляризуються. В хімічних реакціях 2-хлоретанол-1 може віддавати протон, виявляти таким чином кислотні властивості. Тому у спиртів іде розрив С-О і О-Н зв'язків. Крім того на атомі кисню гідроксильної групи спирту є вільні пари електронів. За рахунок цих електронів 2-хлоретанол-1 може також приєднувати протон до атому кисню ОН-групи і виявляти при цьому основні властивості. Отже 2-хлоретанол-1 виявляє кислотно-основні властивості |
+ М ефект виявляють атоми і групи атомів, які мають вільні електронні пари. Зв'язок С-О скорочується і зменшується, зв'язок О-Н додатково поляризується. Це приводить до того, що Н+ швидко відщеплюється у вигляді протону. Електронно-акцепторні замісники збільшують кислотні властивості фенолів. Cl-замісник І-роду, електронно-акцепторний замісник. У фенолів відбувається розрив О-Н зв'язків У фенолів більші кислотні властивості, ніж у спиртів. |
2-Хлоретанол-1 і n-хлорфенол
Мають гідроксильну групу і атом галогену.
Цим обумовлені їх східні властивості. 1. Взаємодія з Ме
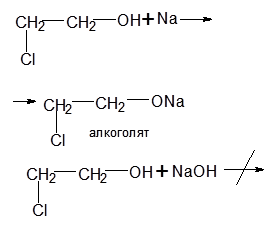
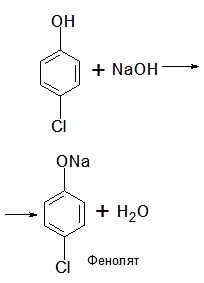
| Реакція гідроксильної групи | |
| 1. Реакція з галогеноводнями | |
|
2-хлорпентанол легко реагує з галогеноводнями і утворює при цьому алкілгалогеніди. --> ЧИТАТЬ ПОЛНОСТЬЮ <-- К-во Просмотров: 377
Бесплатно скачать Реферат: Порівняння властивостей органічних речовин
| |

