Реферат: Рекомбинантные вакцины (Генная инженерия)
Получение рекомбинантных РНК с помощью рибозимов основано на обратимости реакции самосплайсинга (при отсутствии гуанозина или гуаниловых нуклеотидов). Это предоставляет возможность для встраивания интронной РНК в заданный участок другого сегмента РНК (рис. 3). Фрагмент РНК, в который производится встраивание, должен содержать нуклеотидную последовательность, идентичную нуклеотидной последовательности 3'-концевого участка 5'-экзонного района 26S РНК и соответственно комплементарную той нуклеотидной последовательности в интроне, которая отвечает за специфичность прямой реакции. Фрагмент, в который производится встраивание, берется в избытке.
В настоящее время описанная здесь цепь реакций может быть реализована только для интронной РНК, получаемой из предшественника 26S РНК тетрахимены. Однако можно думать, что конструирование новых рибозимов может существенно расширить возможности этого подхода.
1.2.3. СТРАТЕГИЯ КЛОНИРОВАНИЯ ГЕНОВ
Векторные молекулы в обязательном порядке содержат маркерные гены, которые после переноса вектора в клетки-реципиенты сообщают им новые свойства. Это может быть устойчивость к антибиотику, которой до трансформации клетки не обладали, или образование фермента, синтез которого в клетках-реципиентах не происходил. Благодаря таким вновь приобретенным признакам клетки с векторными ДНК могут быть легко найдены в популяции исходных клеток. Одновременно могут быть отобраны те клетки, которые содержат векторы со встроенными в них чужеродными ДНК (рекомбинантные ДНК). Для этого встраивание чужеродной ДНК в вектор производится таким образом, чтобы один из маркерных признаков вектора нарушался. Так, например, если бактериальный вектор несет устойчивость к двум антибиотикам, то чужеродную ДНК встраивают в один
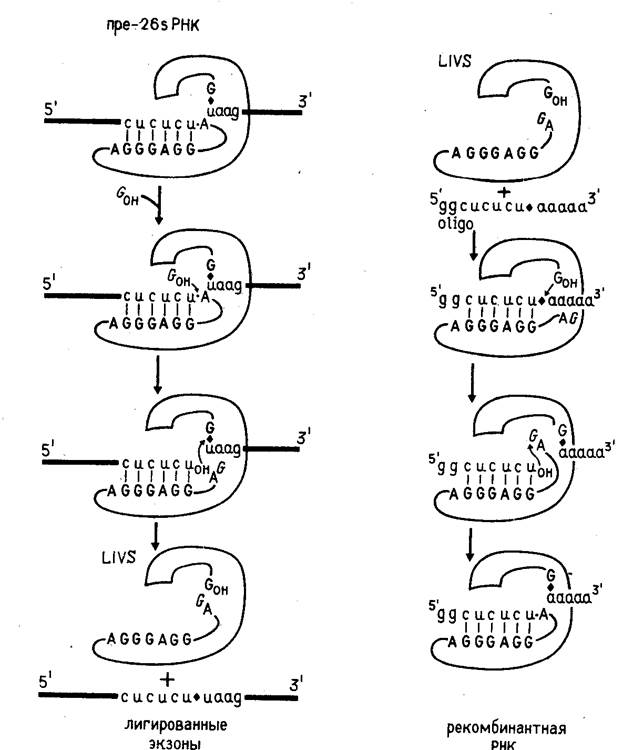
Рисунок 3. Схема прямого и обращенного процесса самосплайсинга.
из генов антибиотической устойчивости. И тогда бактерии с рекомбинантной ДНК, в отличие от бактерий с исходным вектором, могут расти в присутствии только одного из антибиотиков.
Другой весьма распространенный пример связан с наличием в векторной ДНК наряду с генами, сообщающими клетке устойчивость к антибиотикам, фрагмента лактозного оперона, обеспечивающего образование в клетках-реципиентах активного фермента b-галактозидазы. Колонии клеток с таким признаком легко обнаруживаются при выращивании их на твердом агаре, содержащем в качестве субстрата b-галактозидазы 5-бром-4-хлор-3-индолил-b-галактозид (X-gal), поскольку его расщепление приводит к образованию бромхлориндола - красителя, окрашенного в голубой цвет. Если же в ген b-галактозидазы этого вектора встроена чужеродная ДНК таким образом, что этот ген оказался нарушенным, то трансформированные им клетки будут образовывать бесцветные колонии. Само же присутствие рекомбинантного вектора в клетках может быть зафиксировано по их устойчивости к антибиотику.
На следующем этапе среди популяции клеток с рекомбинантными векторами необходимо отобрать индивидуальные клоны, содержащие только интересующие нас гены или их фрагменты. Само собой разумеется, что это в принципе возможно только в том случае, если в исходные клетки проникло в среднем по одной молекуле рекомбинантной ДНК. Способ же отбора клонов в значительной степени зависит от природы клонируемого гена.
По-видимому, самым простым является случай, когда клонируемый ген способен комплементировать ауксотрофную мутацию в штамме-реципиенте. В этом случае клетки высеваются на среду, лишенную вещества, необходимого для роста данного штамма, и только клетки, содержащие рекомбинантную ДНК с искомым геном, способны расти на этой среде. Из таких клонов получают гомогенную культуру клеток, которую используют для получения искомого сегмента ДНК, проделывая все операции в обратном порядке (то есть из клеток выделяют вектор, из него вычленяют необходимый фрагмент ДНК и так далее).
Гораздо чаще для отбора необходимых клонов приходится прибегать к методу ДНК-ДНК- или ДНК-РНК-гибридизации. Для этого необходимо располагать "зондами" (индивидуальными молекулами ДНК или РНК или их фрагментами), комплементарными нуклеотидной последовательности клонируемого гена. Это могут быть специально синтезированные олигодезоксирибонуклеотиды длиной в 15-20 остатков, последовательность которых выбрана на основании полностью или частично известной первичной структуры гена или закодированного в нем белка. Это могут быть кДНК, синтезированные на индивидуальных РНК-копиях данного гена (как таковые или в виде отклонированных, то есть существенно умноженных в количестве фрагментов ДНК). Наконец, это могут быть сами индивидуальные РНК, закодированные в данном гене. Ясно, что во всех случаях "зонды" должны нести радиоактивную метку (обычно 32 Р) с достаточно высокой удельной активностью.
Если же индивидуальный "зонд" недоступен, то применяют методы, которые из большого числа рекомбинантов (106 ) позволяют выбрать сравнительно небольшую группу (около 102 ), включающую рекомбинант с искомым геном. Эта группа подразделяется на подгруппы (например, на 10) по 10 рекомбинантов. Из каждой подгруппы выделяется ДНК, которую используют для синтеза мРНК и последующей трансляции ее с целью обнаружения соответствующего продукта искомого гена.
Трансляция мРНК может быть осуществлена в бесклеточной системе. Однако в случае эукариотических генов мРНК часто переносят в ооциты лягушки (ксенопуса) с помощью техники микроинъекции, где она транслируется. Продукт трансляции обычно обнаруживают с помощью антител.
Далее в подгруппе, где обнаружен искомый ген, тем же методом исследуется каждый клон.
При наличии зонда с чашки Петри, на которой выращены колонии клеток, делается отпечаток (реплика) на нитроцеллюлозном фильтре. Клеткам дают вырасти на фильтре, затем их разрушают, подвергают ДНК щелочной денатурации и фильтр прогревают при 80°С, после чего ДНК необратимо с ним связывается. Фильтр отмывают от примесей и обрабатывают радиоактивным "зондом" в условиях, оптимальных для ДНК-ДНК- или ДНК-РНК-гибридизации. После удаления избытка "зонда" методом ауторадиографии определяют положение клеточного клона, содержащего участок ДНК с нуклеотидной последовательностью, комплементарной "зонду". Этот клон становится затем источником клеток для получения искомого гена или его фрагмента.
Для селекции клонов, несущих необходимый ген, достаточно широко применяются и иммунологические методы. Принцип отбора на первых этапах тот же, что и при использовании ДНК- и РНК-зондов. Далее с колоний с рекомбинантными ДНК делается реплика с помощью полимерной пластинки, на которой закреплены антитела к продукту искомого гена. Положение клонов, вырабатывающих этот белок, определяется также с помощью антител, но уже меченных радиоактивным йодом (125 I).
1.2.4. РАЗНООБРАЗИЕ ВЕКТОРНЫХ МОЛЕКУЛ
Под понятием "вектор" понимается молекула нуклеиновой кислоты, способная после введения в клетку к автономному существованию за счет наличия в ней сигналов репликации и транскрипции.
Векторные молекулы должны обладать следующими свойствами:
1) способностью автономно реплицироваться в клстке-реципиенте, то есть быть самостоятельным репликоном;
2) содержать один или несколько маркерных генов, благодаря экспрессии которых у клетки-реципиента появляются новые признаки, позволяющие отличить трансформированные клетки от исходных;
3) содержать по одному или, самое большее, по два участка (сайта) для различных рестриктаз в разных районах (в том числе в составе маркерных генов), но не в области, ответственной за их репликацию.
В зависимости от целей эксперимента векторы можно условно разделить на две группы: 1) используемые для клонирования и амплификации нужного гена; 2) специализированные, применяемые для экспрессии встроенных чужеродных генов. Вторая группа векторов объединяет векторы, призванные обеспечить синтез белковых продуктов клонированных генов. Векторы для экспрессии содержат последовательности ДНК, которые необходимы для транскрипции клонированных копий генов и трансляции их мРНК в штаммах клеток.
В качестве прокариотических векторов используются плазмиды, бактериофаги; в качестве эукариотических векторов применяют вирусы животных и растений, векторы на основе 2 мкм дрожжей и митохондрий и ряд искусственно сконструированных векторов, способных реплицироваться как в бактериальных, так и в эукариотических клетках (челночные векторы).
Плазмиды - это внехромосомные генетические элементы про- и эукариот, которые автономно реплицируются в клетках. Большинство плазмидных векторов получено на основе природных плазмид ColE1, pMB1 и p15A.
Бактериальные плазмиды делят на два класса. Одни плазмиды (например, хорошо изученный фактор F, определяющий пол у E .coli ) сами способны переходить из клетки в клетку, другие такой способностью не обладают. По ряду причин, и прежде всего для предотвращения неконтролируемого распространения потенциально опасного генетического материала, подавляющее большинство бактериальных плазмидных векторов создано на базе плазмид второго класса. Многие природные плазмиды уже содержат гены, определяющие устойчивость клеток к антибиотикам (продукты этих генов - ферменты, модифицирующие или расщепляющие антибиотические вещества). Кроме того, в эти плазмиды при конструировании векторов вводятся дополнительные гены, определяющие устойчивость к другим антибиотикам.
На рис. 4 показан один из самых распространенных плазмидных векторов E .coli - pBR322. Он сконструирован на базе детально изученной плазмиды E .coli - колициногенного фактора ColE1 - и содержит ориджин репликации этой плазмиды. Особенность плазмиды ColE1 (и pBR322 соответственно) состоит в том, что в присутствии ингибитора синтеза белка антибиотика хлорамфеникола (опосредованно ингибирующего репликацию хозяйской хромосомы) ее число в E .coli возрастает от 20-50 до 1000 молекул на клетку, что позволяет получать большие количества клонируемого гена. При конструировании вектора pBR322 из исходных плазмид был делегирован целый ряд "лишних" сайтов для рестриктаз.
В настоящее время наряду с множеством удобных векторных систем для E .coli сконструированы плазмидные векторы для ряда других грамотрицательных бактерий (в том числе таких промышленно важных, как Pseudomonas , Rhizobium и Azotobacter ), грамположительных бактерий (Bacillus ), низших грибов (дрожжи) и растений.
Плазмидные векторы удобны для клонирования относительно небольших фрагментов (до 10 тыс. пар оснований) геномов небольших размеров. Если же требуется получить клонотеку (или библиотеку) генов высших растений и животных, общая длина генома которых достигает огромных размеров, то обычные плазмидные векторы для этих целей непригодны. Проблему создания библиотек генов для высших эукариот удалось решить с использованием в качестве клонирующих векторов производных бактериофага l.
Среди фаговых векторов наиболее удобные системы были созданы на базе геномов бактериофагов l и М13 E .coli . ДНК этих фагов содержит протяженные области, которые можно делегировать или заменить на чужеродную ДНК, не затрагивая их способности реплицироваться в клетках E .coli . При конструировании семейства векторов на базе ДНК l фага из нее сначала (путем делений коротких участков ДНК) были удалены многие сайты рестрикции из области, не существенной для репликации ДНК, и оставлены такие сайты в области, предназначенной для встраивания чужеродной ДНК. В эту же область часто встраивают маркерные гены, позволяющие отличить рекомбинантную ДНК от исходного вектора. Такие векторы широко используются для получения "библиотек генов". Размеры замещаемого фрагмента фаговой ДНК и соответственно встраиваемого участка чужеродной ДНК ограничены 15-17 тыс. нуклеотидных остатков, так как рекомбинантный фаго -

Рисунок 4. Детальная рестрикционная карта плазмиды pBR322.
вый геном, который на 10% больше или на 75% меньше генома дикого l фага, уже не может быть упакован в фаговые частицы.