Реферат: Термодинамическое и статистическое описание классических равновесных ансамблей
В настоящее время не вызывают сомнений утверждения, лежащие в основе молекулярно-кинетической теории:
1. Все тела состоят из относительно устойчивых частиц (молекул и атомов);
2. Молекулы находятся в постоянном хаотическом движении;
3. Молекулы взаимодействуют друг с другом.
Эти утверждения носят настолько общий характер, что невозможно указать небольшой набор каких-либо конкретных экспериментов, полностью их доказывающих.
В пользу первого положения прежде всего свидетельствуют сами факты существования таких разделов естествознания, как химия и молекулярная физика, в которых на оснолве гипотезы о молекулярном строении вещества делается множество конкретных выводов, прекрасно согласующихся с экспериментом. В физике имеется множество косвенных методов, позволяющих определять форму, размеры и расположение молекул, данные этих методов согласуются друг с другом. Созданный сравнительно недавно туннельный микроскоп позволяет визуализовать отдельные атомы и молекулы, расположенные на гладкой поверхности проводящего кристалла.
Предположение о хаотическом движении молекул впервые было высказано ботаником Броуном, наблюдавшим незначительные перемещения частичек пыльцы цветка, помещенных в жидкость. Методами своей науки Броун убедился в ошибочности своего исходного предположения, что частицы пыльцы являются живыми существами, обладающими способностью самостоятельного движения, и отнес причину их случайных блужданий к передаче импульса в результате случайных ударов со стороны хаотически перемещающихся молекул. Движением молекул объясняется явления диффузии (постепенного перемешивания различающихся веществ вблизи границы их соприкосновения), теплопередачи (постепенное выравнивание температур при соприкосновении горячих и холодных тел), распространения звука и др. В опыте Штерна была осуществлена непосредственная демонсрация движения молекул горячих паров металла и получена информация о скоростях этого движения.
Наличием взаимодействия молекул объясняется факт возможности существования вещества в различных агрегатных состояниях. Природа сил, возникающих между молекулами - электрическая. На больших расстояниях полярные молекулы притягиваются друг к другу как электрические диполи, на малых - притяжения сменяется отталкиванием близкорасположенных ядер (рис. 7_1). Как видно, существует два значения межмолекулярных расстояний, при которых любая пара молекул будет находиться в равновесии: Ro и бесконечность. В природе реализуются оба типа равновесных состояний. Первое относится к конденсированным состояниям вещества (т.е. жидкостям и твердым телам; различие между ними состоит в наличии кристаллической решетки у последних), второе - к газообразным состояниям. Очевидно, что при изменении объемов, занимаемых конденсированным веществом, неизбежно возникновение больших внутренних сил, обусловленных взаимодействиями между молекулами. Возрастание давления газов при изменении объема связано не с наличием сил взаимодействия между его молекулами, а с увеличением частоты ударов молекул о стенки сосуда.
Основные подходы к описанию макроскопических порций вещества. Поскольку вещество состоит из частиц - молекул, возникает очевидное желание получить описание его свойств в результате решения динамической задачи о движении всех частиц. Как уже отмечалось, адекватное описание движения микроскопических частиц возможно лишь на языке вантовой механики. Однако в случаях, когда частицы оказываются почти свободными, описывающие их уравнения квантовой механики переходят в законы движения ньютона. Т.о. возникает принципиальная возможность получить правильное описание поведения вещества в газообразной форме, используя подходы классической физики. Реально подобная динамическая задача не может быть решена из-за фантастически большого числа частиц, образующих макроскопические порции вещества (например, в 1кг молекулярного водорода число молекул составляет ![]()
![]() , т.е. настолько огромно, что одна только проблема записи результатов расчета всех координат оказывается заведомо невыполнимой).
, т.е. настолько огромно, что одна только проблема записи результатов расчета всех координат оказывается заведомо невыполнимой).
Более плодотворным оказался феноменологический подход к созданию теории вещества, состоящий в введении новых термодинамических характеристик, удобных для описания макроскопических ансамблей (массы, давления, температуры, объема и энтропии), и экспериментального исследования связей между ними. Основным результатом такого подхода была формулировка уравнения состояния идеального газа (уравнения Менделеева-Клайперона):
(1) ![]()
и уравнений теплового баланса, долгое время вполне удовлетворявших практическим потребностям теплофизики.
Несмотря на успехи, описанный подход не мог считаться удовлетворительным, поскольку не соответствовал принципу экономии мышления и содержал новые величины и понятия, никак не связанные с уже имевшимися в фундаментальных теориях. В результате был разработан статистический подход, являющийся своеобразным компромиссом между двумя рассмотренными. В его рамках ставится задача вычисления не набора динамических переменных всех частиц системы, а их средних значений. Эти средние сказываются тесно связанными с термодинамическими характеристиками вещества. Т.о. статистический подход позволяет установить более глубокий физический смысл феноменологически введенных термодинамических величин и объяснить природу связывающих их закономерностей.
Распределение Максвелла.
Первым удачным опытом реализации статистического подхода в теории вещества было решение задачи о распределении по скоростям молекул идеального газа (газа, расстояния между молекулами которого значительно превышают размеры молекул, и в котором притяжение молекул играет существенно меньшую роль, чем межмолекулярное отталкивание). Исходными предпосылками, позволившими решить задачу, были:
1.) Газ находится в состоянии термодинамического равновесия (т.е. его макроскопические параметры и средние значения микроскопических параметров не изменяются во времени).
2.) Все столкновения молекул происходят по законам упругого удара (т.е. при каждом столкновении выполняются законы сохранения импульса и механической энергии).
3.) Пространство, заполненное газом, является однородным и изотропным (это требование, например, предполагает отсутствие силы тяжести и каких-либо других внешних силовых полей).
4.) Молекулы обладают тремя степенями свободы (т.е. не способны вращаться и совершать колебаний).
5.) Движение молекул происходит независимо вдоль каждой из координатных осей.
Перечисленные допущения позволили чисто математически (без каких-либо дополнительных физических требований) рассчитать функцию распределения молекул по скоростям ![]() f(v), с помощью которой вероятность обнаружения молекулы, составляющие вектора скорости которой лежат в интервалах
f(v), с помощью которой вероятность обнаружения молекулы, составляющие вектора скорости которой лежат в интервалах
(1) ![]() ,
,
вычисляется по формуле:
(2) ![]() .
.
Найденное Максвеллом распределение имело вид:
(3) ![]() .
.
Соответствующие графики при различных абсолютных температурах приведены на рис. 7_1, из которых видно, что при любых температурах наибольшая вероятность соответствует скоростям молекул, лежащим в области нуля. Увеличение температуры вызывает лишь относительное увеличение доли быстрых молекул. При T->0 распределение локализуется в раионе точки v=0, что означает исчезновение теплового движения молекул.
Из полученного Максвеллом распределения (3) непосредственно следуют выражения, связывающие термодинамические величины (температуру и давление) с механическими (кинетическая энергия и концентрация частиц):
(4) 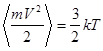 ,
,
(5) ![]() .
.
--> ЧИТАТЬ ПОЛНОСТЬЮ <--