Курсовая работа: Синтез и свойства амилнитрита
Органические нитриты, эфиры азотистой кислоты HNO2 . Содержат одну или несколько групп —О—N=O, связанных ковалентной связью с атомом углерода органического радикала. Низшие алкилнитриты – газы, остальные – бесцветные или желтоватые жидкости, не растворимые в воде, смешиваются с обычными органическими растворителями. Органические нитриты более летучи, чем изомерные им нитросоединения. Физические свойства некоторых органические нитритов приведены в таблице.
СВОЙСТВА НЕКОТОРЫХ ОРГАНИЧЕСКИХ НИТРИТОВ
Соединение Т.кип, °С ![]()
![]()
Метилнитрит CH3 ONO - 12 0,991
Пропилнитрит C3 H7 ONO 48,5 0,935 1,3604
Бутилнитрит C4 H9 ONO 77,8 0,8823 1,3768
Изобутилнитрит C4 H9 ONO 67 0,8699 1,3715
Изопентилнитрит (изоамил-
нитрит) (CH3 )2 CHCH3 CH2 ONO 99,2 0,8828 1,3918
Вращение вокруг связи О—N заметно заторможено (барьер вращения ∆G* 34 кДж/моль), поэтому s-циc - и s-транс -конформеры спектрально различимы. ИК спектр органических нитритов имеет характеристические полосы 1613-1625 и 1653-1681 см-1 (N=O) соотв. для s-цис - и s-транс -форм.
При комнатной температуре органические нитриты медленно разлагаются, на свету низшие органические нитриты могут взрываться. В кислой среде легко гидролизуются; это позволяет использовать органические нитриты в качестве мягких нитрозирующих агентов (для получения малостабильных солей диазония, дезаминирования алкиламинов, нитрозирования фенолов и СН -кислот и т.п.). Органические нитриты, имеющие активированный атом Н при β-углеродном атоме, могут отщеплять HNO2, например:
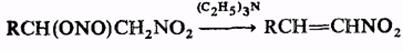
При действии N2 O5 органические нитриты окисляются в нитраты, при действии гидразина или LiAlH4 восстанавливаются в соответствующие спирты. Органических нитриты, содержащие в молекуле более трех атомов С, претерпевают фотохимическую перегруппировку в нитрозосоединения (Бартона реакция), напр.:
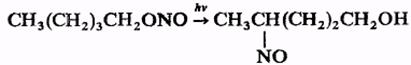
Реакция идет стереоселективно и используется для введения функциональных групп в неактивные участки сложных молекул, например, стероидов.
Получают органические нитриты взаимодействием спиртов с различными нитрозирующими агентами [NaNO2 /H2 SO4 , NaNO2 /Al2 (SO4 )3 , оксиды азота, NOCl/пиридин, NOBF4 ] или взаимодействием алкилгалогенидов с солями HNO2 (наряду с нитросоединениями).
Органические нитриты – высокотоксичные соединения. Этил- и пентилнитриты учащают пульс, понижают кровяное давление, окисляют гемоглобин в метгемоглобин. Органических нитриты обладают сосудорасширяющим и спазмолитическим действием. Изопентилнитрит - противоядие при отравлении синильной кислотой и ее солями.
Органические нитриты – полупродукты в органическом синтезе.
Нитросоединения
Нитросоединениями называют производные углеводородов, в которых один или несколько атомов водорода замещены на нитрогруппу -NO2 . В зависимости от углеводородного радикала, к которому присоединена нитрогруппа, нитросоединения делятся на ароматические и алифатические. Алифатические соединения различают как первичные 1°, вторичные 2 ° и третичные 3°, в зависимости от того к 1 °, 2 ° или 3° атому углерода присоединена нитрогруппа.
Нитрогруппу не следует путать с нитритной группой -ONO. Нитрогруппа имеет следующее строение:

Наличие полного положительного заряда на атоме азота обусловливает наличие у нее сильного -1-эффекта. Наряду с сильным -1-эффектом нитрогруппа обладает сильным -М-эффектом.
Способы получения нитросоединений
Нитрование углеводородов.

Ароматические нитросоединения получают, как правило, прямым нитрованием аренов и ароматических гетероциклических соединений. Нитрометан также может быть получен нитрованием метана.
Синтез нитросоединений из галогенуглеводородов
![]()
Синтез нитрометана из хлоруксусной кислоты
Нитрометан обычно получают из хлоруксусной кислоты по следующей схеме: