Курсовая работа: Синтез нитрата адмантана
Однако синтезировать тринитрокси- и тетранитроксипро-изводные непосредственно из адамантана не удалось. Соответствующие нитраты были получены нитрованием спиртов смесью азотной кислоты с уксусным ангидридом. В табл. 1 приведен ряд нитратов полученных этим способом.
Таблица 1
Нитраты адамантана
| Нитрат | Т. пл., °С | Выход, % |
| 1-AdONO2 | 104-105 | 97.0 |
| 1,3-Ad(ONO2 )2 | 113-114 | 97.1 |
| 1,3,5-Ad(ONO2 )3 | 88 | 70.4 |
| 1,3.5,7-Ad(ONO2 )4 | 139-140 | 95.2 |
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ.
1. Уравнение реакции
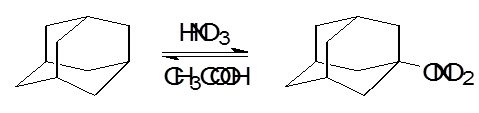
2. Свойства приготовляемого вещества по литературным данным:
Mr 198, Tпл. 1040 С Свойства исходных веществ применяемых при синтезе:
| Название | Формула | Mr | Tпл. ,0 С |
Ткип. , 0 С | Плотность | Примечание |
| Адамантан | С10 H16 | 136 | 209 - 212 | х.ч. | ||
| Азотная кислота | HNO3 | 63 | -20 | 121.6 | 1.5 | 98-100% |
| Уксусная кислота | CH3 COOH | 60 | 16.64 | 117.8 | 1.1403 |
3. Расчет количества веществ, необходимых для синтеза:
Теоретический расчет
(Ad) 136 – 63 (HNO3 )
(Ad) 50 – 23 (HNO3 )
(Ad) 136 – 60 (CH3 COOH)
(Ad) 50 – 22 (CH3 COOH)
Практический расчет
(Ad) 13.6г. – 78г. (HNO3 )
(Ad) 50г. – 286г. (НNO3 )
(Ad) 13.6г. – 26г. (CH3 COOH)
(Ad) 50г. – 96г. (CH3 COOH)
4. Таблица количества веществ, необходимых для синтеза:
|
Количество веществ по руководству | Количество веществ в пересчете на заданное количество(практический расчет) | Количество веществ по уравнению реакции(теоретический расчет) |
Избыток (недостаток) | Примечание | |||||||
| г | мл | моль | г | мл | в пересч. хч. г. | моль | г | моль | г | % | |
| 78 | 52 | 1.2 | 286 | 191 | 280 | 1.3 | 23 | 0.365 | +257 | 91 | 98 – 100% |
| 26.2 | 23 | 0.4 | 96 | 84.5 | 96 | 1.6 | 22 | 0.365 | +74 | 77 | |
| 13.6 | - | 0.1 | 50 | - | 50 | 0.365 | 50 | 0.365 | 0 | 0 | х.ч. |
Реактивы: адамантан 50 г.
азотная кислота 191 мл.
уксусная кислота 84.5 мл