Реферат: Алкалоиды - производные индола
На поперечном срезе видно, что каждая клетка эпидермиса развилась в длинный, до 1 мм волосок, с тупым концом и расширенным булавовидным или луковицеобразным основанием, имеющий сильно утолщенные стенки с порами. Волосок согнут под углом 45°, направлен радиально к центру и тесно прижат к семени. Волоски одревесневшие, легко расщепляются на тонкие фибриллы, окрашиваются раствором флороглюцина в соляной кислоте в малиново-красный цвет. Под эпидермисом лежит несколько слоев сдавленных клеток оболочки семени, а под ними эндосперм из толстостенных многоугольных клеток с капельками жирного масла и алейроновыми зернами неправильной формы, размером 5-30, редко 50 мкм, в поперечнике с глобоидами. Клеточные стенки утолщенные, как бы стекловидные, тонкопористые. Очень тонкие нити протоплазмы (плазмодесмы), пронизывая толщу стенок, связывают между собой содержимое соседних клеток. При окраске разбухшего в воде препарата спиртовым раствором йода содержимое полостей клеток и плазмодесмы окрашивается в бурый цвет, стенки клеток остаются бесцветными. Зародыш состоит из тонкой меристематической ткани. Крахмал и кристаллические включения отсутствуют (15),(18).
2.1.7. Химический состав.
Семена содержат 2-3% алкалоидов, из которых приблизительно 47% приходится на долю стрихнина, и столько же – на долю его диметоксипроизводного – бруцина. В небольших количествах содержатся родственные им вомицин, псевдострихнин, псевдобруцин, a-колубрин, b-колубрин, струксин, которые в сумме составляют не более 0,1%. Из не алкалоидных веществ встречаются хлорогеновая кислота, гликозид логанин, тритерпеноидное соединение циклоарсенол, стигмастерин.
Из листьев выделен алкалоид стрихницин (18).
Стрихнин (I) открыт в 1818 г. Кристаллизуется из этилового спирта в виде бесцветных четырехгранных призм. Трудно растворим в воде, эфире, легче – в бензоле, спирте; t°пл = 286-288°С; [a]D = –104° (в абсолютном спирте), и –139,3° (в хлороформе). Дает много хорошо кристаллизующихся солей, что позволяет использовать его в качестве оптически активного основания для разделения рацематов (1),(2).

Бруцин (II) открыт в 1818 г. Кристаллизуется из разбавленного этилового спирта в виде моноклинных призм, представляющих собой тетрагидрат. Трудно растворим в горячей воде, легко – в спирте, хлороформе, почти не растворим в эфире; тетрагидратная форма плавится при t° = 105°С, безводный алкалоид – при 178°С; [a]D = +119-127° (в хлороформе). Дает много кристаллических солей с азотной кислотой (2).
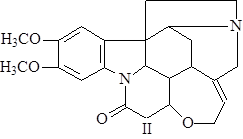
Вомицин (III) впервые выделил Гмелин в 1929 г. из маточников, оставшихся после выделения стрихнина; t°пл = 282°С; [a]D = +80,4° (этанол) (1).

Псевдострихнин (IV) обнаружен Варнатом в 1931 г. t°пл = 266-268°С; [a]D = –58° (этанол), и –85,9° (хлороформ) (1).

a-колубрин (V) открыл Варнат в 1931 г. t°пл = 184°С; [a]D = –76,5° (80% этанол) (1),(2).

b-колубрин (VI) открыл Варнат в 1931 г. t°пл = 222°С; [a]D = –107,7° (80% этанол) (1),(2).

2.1.8. Биосинтез стрихнина.
Стрихнин является монотерпеноидным индольным алкалоидом, и синтезируется из их общего предшественника – стриктозидина (винкозида) (I) (10).
В биосинтезе стрихнина можно выделить несколько стадий:
На первой стадии происходит разрыв пиранового кольца (II), с отщеплением глюкозы, и последующим образованием центрального метаболита целого ряда алкалоидов – гизосхизина (III) (19).

На следующей стадии гизосхизин претерпевает метилирование с увеличением боковой цепи на один углеродный атом и образованием соединения, состоящего из 21 атома углерода (IV) (20).

Таким образом, осуществляется переход от С20 -соединений к С21 -соединениям – предшественникам группы стрихнина.

Затем происходит многоступенчатая перегруппировка по типу преакуаммицина, в результате которой получается С21 -аналог преакуаммицина (V), и далее, после замыкания лактамного (С) и оксепинового (G) циклов образуется стрихнин (VI) (21),(22).
2.1.9. Доказательство строения стрихнина.
Уже в самом начале изучения строения стрихнина и бруцина была отмечена близость свойств этих оснований, которая в ряде случаев доходила до полной идентичности. Это навело исследователей на мысль, что бруцин является диметоксипроизводным стрихнина. Это предположение было подтверждено окислением хромовой кислотой в определенных условиях, при котором получался один и тот же продукт – т.н. кислота Ханссена (I) – продукт разрушения ароматического кольца алкалоидов (1).

При нагревании алкалоидов со спиртовой щелочью происходит присоединение воды и образование стрихниновой и бруциновой кислоты (II), которые при действии кислот легко переходят обратно в стрихнин и бруцин. Это указывает на наличие в молекуле лактамной группировки, разрушающейся в щелочном растворе (1).

Было проведено множество экспериментов по окислению стрихнина различными окислителями. Наиболее важно окисление азотной кислотой, при котором происходит образование динитрострихнона. Долгое время его считали производным хинолина или изохинолина, но при дальнейшем окислении вещества был получен динитроизатин (III), что доказывало наличие индольного ядра в молекуле (2).

Далее, было доказано, что один из кислородных атомов имеет карбонильный характер, связан с азотом, индифферентен, и в то же время нейтрализует связанный с ним атом азота. Второй атом кислорода также индифферентен (2).
Стрихнин и бруцин дают бензилиденовые производные, реагируют с азотистой кислотой, давая изонитрозопроизводные (IV). Эти реакции доказывают наличие реакционноспособной метиленовой группы (1).

Алкалоиды содержат одну двойную связь, которая легко гидрируется с образованием дигидрострихнина и дигидробруцина. При более энергичном восстановлении были получены тетрагидрострихнин, стрихнидин, дезоксистрихнин, дигидрострихнолин (1).
Исследования формулы стрихнина продолжались более ста лет со времени его открытия, и только в 1950 г. была предложена структурная формула, которая объясняла все его превращения. Эта структура была подтверждена в 1954 г. Вудвордом (США) с помощью синтеза (1).
2.1.1 0. Качественный анализ.
Фармакопейный качественный химический анализ сырья чилибухи заключается в открытии стрихнина и бруцина.
Хлороформное извлечение порошка семян фильтруют через фильтр с безводным сульфатом натрия, делят на 2 части и упаривают на водяной бане досуха. К одной части сухого остатка прибавляют раствор бихромата калия и осторожно по стенкам чашки – концентрированную серную кислоту. При покачивании чашки появляются красно-фиолетовое окрашивание – стрихнин. К другой части сухого остатка прибавляют концентрированную азотную кислоту, появляется оранжево-красное окрашивание – бруцин. Также можно проводить анализ на срезах семян чилибухи: при смачивании обезжиренного среза каплей концентрированной серной кислоты со следами ванадата аммония содержимое клеток тотчас же окрашивается в фиолетовый цвет. При смачивании среза каплей дымящей азотной кислоты, содержимое клеток окрашивается в оранжево-желтый цвет (15).
Нефармакопейные реакции на стрихнин.