Реферат: Изучение трехмерной структуры с помощью рентгеновской дифракции и реконструкции изображения
Например, отдельные части цитохром с-оксидазы возвышаются над поверхностью бислоя на 50 А 1314, 466] ; такая же картина наблюдается для ацетилхолинового рецептора. Напротив, порин и бактериородопсин почти не выдаются над поверхностью мембран. На рис.3.3 представлена структура цитохром с-оксидазы, полученная с низким разрешением.
2.2 Три примера структурных исследований мембранных белков
Рассмотрим три примера изучения интегральных мембранных белков, иллюстрирующие большое разнообразие используемых для этого методов. Наиболее известными структурами являются реакционные центры R. viridis и R. sphaeroides, исследование которых с помощью рентгеновской дифракции было весьма успешным. Еще одна наиболее полно изученная структура - бактериородопсин Н. halobium; для его исследования применялся метод реконструкции изображения, а также другие подходы. Порин и родственные белки наружной мембраны Е. соЧ изучали в основном с помощью генетических и молекулярно-биологических методов, позволяющих идентифицировать функционально важные участки.
3. Структура фотосинтетических реакционных центров ft. viridis и ft. sphaeroides
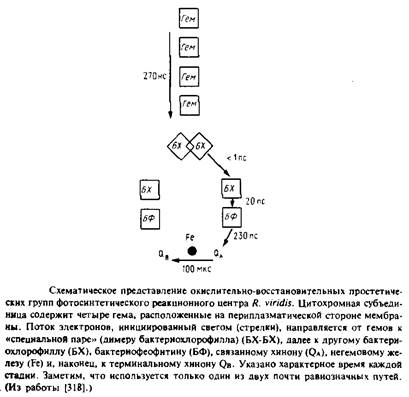
Фотосинтетические реакционные центры представляют собой комплексы белков с пигментами; в них происходит первичное разделение зарядов в фотосинтетических мембранах. Лучше всего охарактеризованы комплексы из пурпурных несерных бактерий; они обычно состоят из трех белковых субъединиц - Н, М и L. Реакционный центр Rhodopseudomonasviridis имеет также четвертую субъединицу - цитохром с-типа. Простетическими группами этого комплекса являются четыре гемогруппы, четыре бактериохлорофилла Ь, два бактериофеофитина, одно негемовое железо, один менахинон и одинубихинон. Под действием света электрон переходит от первичного донора электронов, так называемой "специальной пары" - молекул бактериохлорофилла, образующих димер, к бактериофеофитину, а затем к первичному хиноновому акцептору QA . В конце концов электрон восстанавливает вторичный акцептор Qb в ходе реакции, при которой протоны поступают из раствора на восстановленный хинон. Qbнаходится в равновесии с хинонным пулом в би-слое. Окисленный первичный донор электронов, "специальная пара", восстанавливается цитохромом с-типа. Поскольку цитохром и хинон расположены на противоположных сторонах фотосинтетической мембраны, светозависимый электронный транспорт электроге-нен и генерирует трансмембранную разность потенциалов.
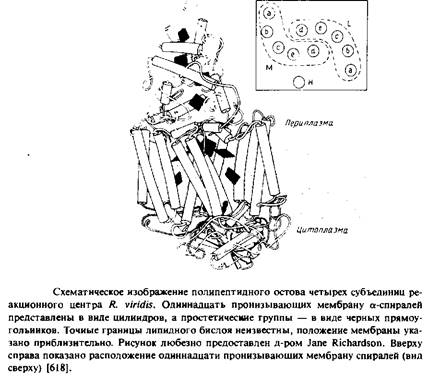
Суммарная мол. масса реакционного центра из R. viridisсоставляет примерно 150 ООО, а кажущаяся мол. масса субъединиц - 38 ООО, 35 ООО, 28 ООО и 24 ООО. Заметим, что электрофорез в ПААГ-ДСН дает неправильные молекулярные массы для Н, М и Lсубъединиц; об этом свидетельствуют данные о числе аминокислотных остатков в каждом полипептиде, полученные при секвенировании ДНК. Очищенный комплекс был закристаллизован с использованием сульфата аммония как осаждающего агента в присутствии детергента N. N-диме-тилдодециламин-М-оксида и органического амфифильного соединения гептан-1,2,3-триола. Кристаллы были в достаточной степени упорядочены и фотохимически активны. Структура этого четырехсубъединичного белка была установлена с разрешением около 3 А. Детергент в кристаллах не упорядочен, поэтому невозможно точно определить положения границ погруженных в мембрану участков. Размеры комплекса - 30 х 70 х 130 A. L - и М-субъединицы содержат по пять трансмембранных а-спиральных участков, а у Н-субъединицы такой участок только один.
Итак, все трансмембранные области этого белкового комплекса имеют а-спиральную конфигурацию. Длина каждого а-спирального сегмента составляет примерно 40 А, этого достаточно для пересечения мембраны.
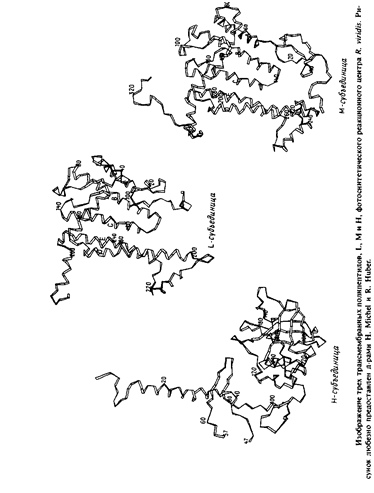
Структура белкового комплекса из R. viridis напоминает сэндвич. L - и М-субъединицы уложены одинаковым образом и расположены в центре сэндвича. Они пересекают бислой и связаны со всеми простетическими группами, за исключением гемов. Сегменты L и М, которые соединяют трансмембранные сегменты по обе стороны мембраны, участвуют в связывании цитохрома и Н-субъединиц. Цитохром образует "шапочку" на наружной поверхности бислоя, а гидрофильная часть субъединицы Н - аналогичную структуру на цитоплазматической поверхности. Трансмембранная а-спираль на N-конце Н-субъединицы контактирует с цитохромом на противоположной стороне мембраны.
Эти межмолекулярные взаимодействия в кристаллах осуществляются между участками Н-субъединицы и цитохромом, которые в норме контактируют с водой. Возможно, эти два белка, образующие гидрофильные "шапочки", способствуют формированию высокоупорядоченных кристаллов.
Отметим некоторые важные структурные особенности рассматриваемого комплекса.
Все 11 трансмембранных участков представляют собой а-спирали, а составляющие их аминокислоты в большинстве своем неполярны. В каждой из трансмембранных спиралей L-и М-субъединиц имеется последовательность длиной не менее 19 остатков, не содержащая никаких кислых или основных аминокислот.
Трансмембранные спирали в каждой из субъединиц L или М обычно антипараллельны своим соседям, но спирали сие параллельны друг другу. Наклон спиралей к нормали к плоскости мембраны не превышает 25°, за исключением спирали d, которая наклонена к нормали под углом 38°. Длина спиралей варьирует от 24 до 30 остатков.
Те участки L - и М-субъединиц, которые соединяют трансмембранные сегменты, образуют уплощенные структуры по обе стороны мембраны, которые могут контактировать с двумя гидрофильными субъединицами.
Заряженные аминокислоты в субъединицах L и М распределены асимметрично, так что полярные концы трансмембранных спиралей и соединяющие их участки заряжены более отрицательно на периплазматической стороне мембраны, чем на цитоплазматической. Это создает определенные энергетические выгоды, поскольку мембранный потенциал отрицателен на цитоплазматической стороне.
Все эти структурные данные ценны также в том отношении, что они помогают понять фотохимию этого важного комплекса.
Хотя редокс-центры, по-видимому, создают два параллельных пути переноса электронов от "специальной пары", эти две ветви не идентичны, и при переносе электронов через мембрану, вероятно, используется только одна из них. Фотосинтетические пигменты жестко фиксируются в определенном месте за счет гидрофобных взаимодействий и водородных связей с белком и вряд ли перемещаются во время реакции.
Перенос электрона от "специальной пары" к бактериофеофитину происходит очень быстро; это согласуется с тем, что участвующие в процессе простетические группы находятся друг от друга на расстоянии вандерваальсового радиуса. Характерное время переноса электрона от бактериофеофитина к Qaсоставляет 230 пс, и центры этих двух групп разделены расстоянием около 14 А. Однако изопреноидная боковая цепь хинона непосредственно контактирует с бактериофеофитином.
Перенос электрона от цитохрома, сопровождающийся восстановлением специальной пары, происходит медленно, за 270 не, в соответствии с тем, что центр ближайшего гема расположен от центра специальной пары на расстоянии 21 А. Из-за этого, в частности, замедляется перенос электрона.
Перенос QA Qbможет осуществляться при участии негемового железа, хотя оно, по-видимому, не является необходимым для этого процесса. Хинон Qbсвязывается слабо и утрачивается в процессе приготовления образца. Возможно, функциональная роль Н-субъединицы состоит в связывании QB .
Структура трехсубъединичного реакционного центра Rhodobactersphaeroides, также установленная методом рентгеновской дифракции с разрешением 2,8 А, очень похожа на структуру реакционного центра R. viridis. Модельные исследования позволяют предположить, что негемовое железо и хиноны расположены на уровне полярных концевых групп фосфолипидов внутри бислоя, хотя они полностью окружены белками. Специальная пара бактериохлорофилла находится примерно на 5 А ниже полярных липидных головок. Одиннадцать трансмембранных спиралей упакованы столь же плотно, как аминокислотные остатки внутри водорастворимых белков. Те аминокислотные остатки в трансмембранном участке, которые контактируют с белком, обычно гидрофобны; такая же картина характерна и для соответствующих аминокислот водорастворимых белков. Полярные связи между трансмембранными спиралями весьма немногочисленны. Трехсубъединичная структура стабилизируется за счет:
1) взаимодействия между экспонированными наружу участками субъединиц;
2) благоприятных дипольдипольных взаимодействий между антипараллельными плотноупакованными а-спиралями;
3) вандерваальсовых взаимодействий между плотноупакованными спиралями;
4) связывания одного атома железа с четырьмя гистидиновыми остатками d - и е-спиралей L - и М-субъединиц. Отсутствием полярных взаимодействий между трансмембранными спиралями этот комплекс отличается от большинства моделей бактериородопсина, обсуждаемых в следующем разделе.
В заключение отметим, что реакционные центры бактерий сходны с реакционными центрами фотосистемы II высших организмов, которые ответственны за окисление воды и выделение кислорода. Он содержит единственную ковалентно связанную простетическую группу ретиналь, которая с помощью шиффова основания присоединена к лизину-216. Этот белок выполняет функцию фотохимического протонного насоса, создающего разность электрохимического потенциала протонов, которая затем используется клеткой для транспорта растворимых веществ и синтеза АТР. При поглощении ретиналем одного протона индуцируется ряд превращений, в том числе т/? анс-г/нс-изомеризация по связи С13-С14 ретиналя и депротонирование азота шиффова основания; это приводит к электрогенному переносу одного или двух протонов из клетки наружу.
Поскольку insitu этот белок образует высокоупорядоченную двумерную кристаллическую решетку, для установления его трехмерной структуры можно использовать методы реконструкции изображения. Белок имеет относительно малые размеры и выполняет весьма важную функцию протонного насоса, а за всеми превращениями ретиналя можно следить оптическими методами. Все это стимулировало детальные исследования механизма функционирования бактериородопсина. Фотохимические свойства шиффова основания ретиналя изучены довольно хорошо, однако как они влияют на белок и что вызывает перемещение протонов - неизвестно. Структурные данные тоже не пролили свет на механизм функционирования белка, хотя и были предложены модели протонной "эстафеты" или цепочки трансмембранных водородных связей. С другой стороны, функционально-механистические исследования тоже не дали никаких указаний, которые помогли бы в интерпретации структурных данных.
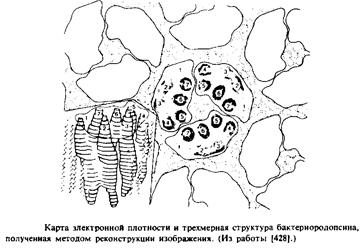
Структурный каркас бактериородопсина был построен методом реконструкции изображения с использованием электронно-микроскопических данных; это случай наиболее успешного применения данного подхода. Карты электронной плотности позволяют получить разрешение лучше, чем 3,7 А, в плоскости мембраны и около 14 А в плоскости, перпендикулярной бислою. На рис.3.7 представлены одна из карт электронной плотности и соответствующая трехмерная модель. Белок состоит из тримеров, при этом каждый полипептид предстает в виде образования из семи цилиндров, пронизывающих мембрану и примерно перпендикулярных ее плоскости. Обычно считают, что эти цилиндры представляют собой а-спиральные участки белковой молекулы. Их длина по оценкам равна 45 А, что согласуется с рентгеноструктурными данными о том, что толщина пурпурной мембраны составляет примерно 49 А. Если полипептид действительно находится в а-спиральной конфигурации, то эта величина должна соответствовать 30 остаткам, поскольку расстояние между остатками вдоль оси а-спирали равно 1,5 А. Следовательно, в семи предполагаемых а-спиралях содержится более 80% всех аминокислотных остатков. И действительно, как показывают данные КД, большая часть белковой молекулы находится в а-спиральной конфигурации, хотя имеются также участки, образующие 3-слой.