Реферат: Изучение трехмерной структуры с помощью рентгеновской дифракции и реконструкции изображения
1) определение аминокислотной последовательности;
2) протеолиз и иммунологические методы для выявления тех участков белка, которые находятся за пределами бислоя, и установления их ориентации относительно внутренней и наружной сторон мембраны.
Все построенные модели сходны в интерпретации общей укладки и топологии молекулы. На рис.3.8 представлена модель, аналогичная предложенной Энгелманом и др. Установлено, что для пересечения неполярной части бислоя спираль должна содержать 21 аминокислотный остаток, и в белковой молекуле действительно имеется семь участков примерно такой длины с преобладающим содержанием неполярных аминокислот. Полагают, что они и образуют семь а-спиралей, наблюдаемых на карте электронной плотности.

Эти а-спирали обычно обозначаются буквами А, В, С, D, E, F, G, начиная с N-конца. Каково соответствие между ними и семью спиралями, выявленными с помощью электронно-микроскопических исследований, - неизвестно. Этот вопрос неоднократно обсуждался, и здесь существуют разные мнения. Почти не вызывает сомнений, что общая топология, представленная на рис.3.8, адекватна. Разные модели, описанные в литературе, в каких-то отношениях могут существенно различаться. Это касается, в частности, длины нескольких спиралей, расположенных внутри бислоя, которая варьирует в разных моделях в пределах 10 остатков. Несмотря на эти разногласия, по главным особенностям достигнут консенсус, хотя говорить о единодушии нельзя. Эти особенности следующие.
Участки белка, пересекающие бислой, имеют форму а-спиралей и в целом неполярны. Спирали, вероятно, пронизывают всю толщу мембраны, а не только неполярную часть бислоя. Спирали перпендикулярны поверхности мембраны и упакованы так, что расстояние между их центрами составляет 10 А.
Заряженные и полярные аминокислотные остатки расположены в основном в участках, соединяющих трансмембранные спирали. В той части белковой молекулы, которая погружена в неполярную часть бислоя, имеется до девяти ионизируемых остатков в зависимости от того, где расположены его границы. По-видимому, для стабилизации структуры они должны быть каким-то образом нейтрализованы. Возможно, они образуют ионные или водородные связи с остатками, расположенными в другой части полипептидной цепи. Этот момент может оказаться полезным при обсуждении вопроса о характере упаковки разных спиралей в мембране. По-видимому, ионизируемые остатки, располагающиеся внутри мембраны, имеют структурное и/или функциональное значение. Пример тому - остаток Lys-216, с которым связывается ретиналь. Большинство заряженных аминокислотных остатков, локализованных в экспонированных в раствор участках белка, располагаются вблизи цитоплазматической поверхности или непосредственно на ней.
Примерно в середине спиралей В, С и F расположены по три остатка пролина, однако спирали при этом не выглядят сильно изогнутыми.
Наблюдается асимметричное распределение ароматических аминокислот: многие остатки тирозина и почти все остатки триптофана находятся вблизи наружной стороны мембраны. Значение этого феномена неизвестно.
N-Конец располагается у наружной стороны мембраны, а С-конец - у внутренней.
С-Концевой участок, по-видимому, имеет форму статистического клубка и может подвергаться протеолизу без нарушения функций белка.
Лизин-216 связан с простетической группой - ретиналем и расположен примерно в середине спирали G.
3.1 Вывернутый белок
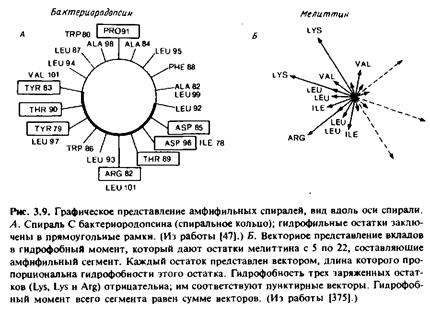
Относительно структуры бактериородопсина можно сделать весьма интересный вывод: его полипептидная цепь уложена так, что полярные или заряженные остатки, находящиеся в семи трансмембранных участках, оказываются обращенными внутрь глобулы, а неполярные контактируют с мембранными липидами. Глобула по существу "вывернута", если сравнивать ее с белками, в которых большинство неполярных остатков спрятаны внутри структуры, а полярные обращены наружу. Этому есть разумное объяснение, и об этом же свидетельствуют некоторые экспериментальные данные, в первую очередь данные по рассеянию нейтронов. В основе упомянутого метода лежит существенное различие между рассеянием на атомах водорода и дейтерия. Дейтерированные валин и фенилаланин включали путем биосинтеза в бактериородопсин и затем, используя разностный метод Фурье, устанавливали распределение этих аминокислот в проецируемой структуре пурпурной мембраны. Приняв общепринятые допущения о последовательности предполагаемых спиральных участков, при построении соответствующей модели обнаружили, что если смотреть вдоль оси спирали, то для каждой спирали остатки валина будут располагаться на сторонах, противоположных заряженным и полярным группам, а остатки фенилаланина - преимущественно на противоположной валину стороне. По данным нейтронного рассеяния, остатки валина преимущественно обращены к мембранным липидам, поэтому был сделан вывод, что заряженные и полярные остатки группируются внутри белка. Заметьте, что этот результат не зависит от конкретного расположения участков полипептида на электронно-микроскопической карте.
Другой подход основан на использовании гидрофобного фотореактивного зонда 125 1-ТИД. Этот реагент внедряется в гидрофобную сердцевину мембраны и при фотолизе неспецифически реагирует с наиболее доступными боковыми группами аминокислот. Это его свойство может использоваться для локализации тех участков белковой молекулы, которые обращены к липидам. По крайней мере в двух случаях, в том числе в случае бактериородопсина, отмечалось включение метки в специфические, периодически расположенные участки полипептидной цепи, при этом метка включалась через каждые три или четыре остатка.
Если такой характер мечения отражает только долю боковых групп, обращенных к мембранным липидам, то мы сможем установить, какая сторона предполагаемого а-спирального участка контактирует с липидами. Поскольку на один виток спирали приходится 3,6 остатка, то наблюдаемая периодичность может иметь место только в том случае, если зонд контактирует лишь с одной стороной спирали. Данные по спирали С в бактериородопсине согласуются с представлением о вывернутой структуре этого белка и тоже свидетельствуют о том, что соответствующая часть полипептида имеет спиральную конфигурацию. В целом можно сказать, что концепция вывернутых интегральных мембранных белков весьма разумна, однако экспериментальное ее обоснование пока недостаточно. Напомним, что, согласно моделям фотосинтетического реакционного центра, в сердцевине бислоя находится очень мало ионизируемых остатков или они отсутствуют там вообще.
3.2 Расположение спиралей в бислое и их соединение
Ситуация, которая сложилась при изучении бактериородопсина, весьма необычна в том смысле, что при промежуточном уровне разрешения удается установить некоторые структурные детали, но этого разрешения недостаточно для однозначного определения конфигурации белка в бислое. Все попытки, которые предпринимались здесь до сих пор, скорее смогли выявить ограничения использовавшихся методов, чем выяснить принципы структурной организации мембранных белков. Применялись следующие методы.
Теоретический анализ, направленный на поиск такой конфигурации спиральных участков, при которой происходит оптимальная нейтрализация зарядов благодаря образованию ионных связей внутри бислоя, а также на оценку длины полипептидных участков, соединяющих спирали.
Нейтронное рассеяние с использованием дейтерированных аминокислот и данных об аминокислотном составе каждого спирального участка.
Улучшение разрешения в плоскости мембраны с использованием метода. реконструкции изображения и электронной дифракции.
Определение рентгеновского рассеяния до и после протеолитического расщепления N-концевого пептида с целью идентификации на карте электронной плотности остатков, расположенных на N-конце.
Исследование с помощью нейтронного рассеяния бактериородопсина, реконструированного из протеолитических фрагментов, один из которых был дейтерирован.
Нейтронное рассеяние с использованием дейтерированного ретиналя, включенного либо путем замещения, либо биосинтетически. Ретиналь был присоединен к Lys-216 в спирали G. Считается, что он расположен внутри бислоя под углом 75° по отношению к нормали, т.е. почти параллельно поверхности мембраны.
Фотохимическое сшивание с использованием фотореактивного производного ретиналя. Этот метод позволяет выявить ближние взаимодействия.
Каждый из этих подходов имеет свои ограничения, и в этом смысле они не согласуются между собой. Существует 5040 возможных способов размещения семи спиралей в семи бороздках, и до настоящего времени эти методы давали противоречивые ответы на вопрос даже о наиболее вероятном их расположении.
4. Структура поринов
Порины - это основной класс белков, обнаруженных в наружной мембране кишечных бактерий. У Е. coli и Salmonellatyphimurium выявлены три порина: OmpF, OmpC и PhoE. Эти белки имеют мол. массу примерно 35 ООО и гомологичные аминокислотные последовательности. Порины экстрагируются из наружной мембраны с помощью ДСН в виде стабильных тримеров; их можно встроить в фосфолипидные бислои с образованием неспецифичных пор, способных пропускать малые гидрофильные молекулы. По-видимому, именно они придают наружной мембране бактерий свойство молекулярного сита, Позволяя питательным веществам проникать внутрь клетки, а отходам - выводиться наружу через неспецифические каналы.
Были проведены обширные структурные исследования белка OmpF, известного также под названием "матриксный порин"; в настоящее время осуществляется кристаллографический анализ, который позволит получить его структуру с высоким разрешением. Однако уже сейчас можно сделать вывод, что структура OmpF сильно отличается от структуры как бактериородопсина, так и полипептидов, образующих фотосинтетический реакционный центр. Судя по данным о первичной последовательности, в молекуле нет никаких длинных гидрофобных участков, которые можно было бы идентифицировать как трансмембранные, и в среднем в ней содержится больше полярных аминокислот, чем неполярных. Однако трехмерная электронно-микроскопическая реконструкция изображения с использованием кристаллических пластинок реконструированного порина показала, что белок пронизывает бислой, причем за пределы мембраны выходят лишь небольшие участки молекулы. Методом негативного контрастирования были выявлены каналы, образуемые тримерами. Отдельные молекулы порина образуют у внутренней поверхности каналы, которые в середине бислоя сливаются в одиночный канал, открывающийся наружу. Есть и другие данные, свидетельствующие о том, что порин, несмотря на отсутствие в его молекуле гидрофобных участков, является трансмембранным белком. Иногда этот белок выполняет роль рецептора для бактериофага, а также проявляет сродство к компонентам клеточной стенки на периплазматической стороне. Очищенный порин можно встраивать в фосфолипидные бислои с образованием потенциалчувствительных каналов.
Данные инфракрасной спектроскопии, кругового дихроизма и широкоугольной диффузионной рентгеновской дифракции свидетельствуют о том, что две трети длины молекулы образует /3-слой, а на долю а-спиралей приходится небольшая часть длины молекулы. Кроме того, эти исследования показывают, что /3-цепи антипараллельны, ориентированы перпендикулярно плоскости мембраны н имеют среднюю длину 10-12 остатков, которых достаточно для пересечения неполярной области мембраны. Способ укладки /3-цепей можно установить лишь с помощью рентгеновской дифракции. Как показывают модельные исследования, /3-цепи могут быть уложены так, что образуется /3-цилиндр, при этом полярные и заряженные аминокислотные остатки выстилают стенки наполненных водой каналов.
Все известные о структуре порина данные показывают, что гидрофобная а-спираль не является его необходимым трансмембранным элементом. Это означает, что наиболее распространенные способы предсказания структуры трансмембранных белков имеют свои ограничения, поскольку они основываются на предположении, что пересечь бислой могут только гидрофобные сегменты. Точная структура порина до сих пор неизвестна; неясно также, сходна ли она со структурой других мембранных белков. Впрочем, имеются и другие белки наружной мембраны бактерий, которые характеризуются высоким содержанием ^-структур. Один из них - белок ОтрА, который тоже является рецептором для фагов, но, вероятно, не существует в виде отдельных тримеров и не образует поры. Другой белок такого рода - LamB, являющийся рецептором бактериофага лямбда; он функционирует как специфичный канал, через который осуществляется диффузия мальтодекстринов.