Статья: Химическая кинетика и равновесие в гомогенных системах
Выражаем через полученное значение величину Кс:
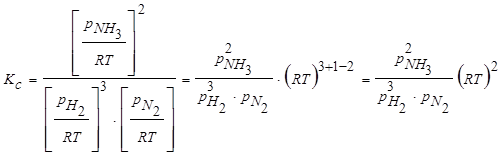 .
.
Или можно записать другим образом:
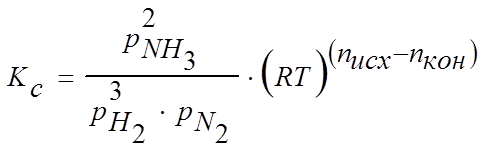
После незначительных преобразований получим:
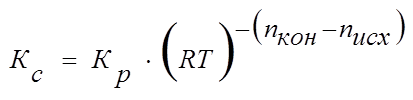
или
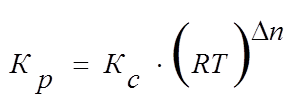 ,
,
где ![]() - разность коэффициентов в уравнении реакции
- разность коэффициентов в уравнении реакции
![]() .
.
Для реакций, протекающих без изменения объема получаем:
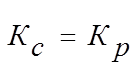 .
.
Существует связь между изменением изобарно–изотермического потенциала химической реакции и константой равновесия, выраженной через парциальное давление компонентов А, В, С, D, Е при равновесии.
Для температуры 298 она выглядит следующим образом:
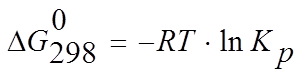 .
.
Если ![]() , то
, то ![]() ; если
; если ![]() , то
, то ![]() и прямая реакция практически необратима в стандартных условиях: если
и прямая реакция практически необратима в стандартных условиях: если ![]() , то
, то ![]() и обратная реакция практически необратимая.
и обратная реакция практически необратимая.
Направление смещения положения химического равновесия в результате изменения внешних условий определяется принципом Ле Шателье:
если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то в системе усиливаются те процессы, которые стремятся свести это воздействие к минимуму.
Влияние концентраций реагирующих веществ на состояние
равновесия
При контактном способе получения Н2SO4 окисление SO2 в SO3 в присутствии катализатора (Pt или V2O5) идет по уравнению:
![]() .
.
Если в эту равновесную систему добавить извне О2, то в системе усиливается процесс, стремящийся понизить концентрацию О2. Таким процессом является прямая реакция SO2 с О2 с образованием SO3. Таким образом, равновесие в системе сместится в сторону образования SO3. К этому же выводу можно прийти при анализе выражения для константы равновесия:
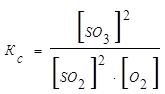 .
.
При увеличении концентрации О2 (знаменатель в этом выражении) должна возрасти концентрация SO3 (числитель). Это следует из того, что Кс=const. Таким образом, повышение концентрации O2 сдвинет равновесие к более полному использованию SO2 и к большему выходу SO3.
Влияние давления на состояние равновесия
Давление имеет существенное значение при реакциях между газами.
В результате увеличения давления повышается концентрация реагирующих веществ и, соответственно, скорость реакции.
Рассмотрим возможные случаи.