Билеты: Гомогенное химическое равновесие
1. Рассчитайте сродство (-ΔrGt) железа к кислороду воздуха, Po2 =2,0266*104 Па при 1000К, если константа равновесия реакции 2Fe+O2 ![]() 2FeO при этой температуре равна 2,450*1020 Па-1 .
2FeO при этой температуре равна 2,450*1020 Па-1 .
2. Константа равновесия реакции H2 +I2 ![]() 2HI при 717К равна 46,7. Определите кол-во разложившегося HI при нагревании 1моль HI при 717К.
2HI при 717К равна 46,7. Определите кол-во разложившегося HI при нагревании 1моль HI при 717К.
3. Вычислите при температуре 298К константу равновесия реакции CO+0,5O2 =CO2 по стандартной энергии Гиббса.
Критерии оценивания
Данная к/р оценивается в 45 баллов. №1-10 баллов, №2-15 баллов, №3-20 баллов.
Наиболее характерные ошибки:
- использование неправильных размерностей величин;
- ошибки при выводе ур-ния Кс реакции;
- неправильное решение квадратного ур-ния и использование его отрицательных корней (для нахождения кол-ва моль прореагировавшего в-ва);
- ошибки при счёте;
- использование неверных справочных значений(необходимо использовать величины, выраженные в Дж/моль, Дж/моль*К или кДж/моль);
- следует учесть, что энтальпия реакции образования простых веществ равна 0;
- для расчета стандартной энергии Гиббса необходимо значение энтропии реакции перевести в кДж/моль;
- если реакция проводится в стандартных условиях, то необходимо использовать PO =0,101Мпа=101,3кПа.
Решение задач
№1.
2Fe+O2 ![]() 2FeO
2FeO
ΔG=-RTlnKp+RTϳ(Pν і і исх.)
ΔG=-8,314*1000ln(2,450*1020 )+8,314*1000ln(2,0266*104 )= -390324-82447=-472,77 кДж/моль.
Ответ. (-ΔrGt)=472,77 кДж/моль.
№2
2HI![]() H2 +I2
H2 +I2
исх. 1моль 0 0
Реак. 2х х х
Равн. 1-2х х х
Кс=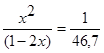
46,7x2 =1-4x+4x2
42,7x2 +4x-1=0
D=186,8
x1 =![]() (моль)
(моль)
2x=0,227 (моль)
Ответ. Разложилось 0,227 моль HI.
№3
![]()


Все необходимые значения станд.![]() для CO2 , O2 и CO берутся из справочника физико-химических величин.
для CO2 , O2 и CO берутся из справочника физико-химических величин.

ΔV-приращение числа молей во время реакции.
Для реакции CO+0,5O2 =CO2
ΔV=1-(1+0,5)= -0,5
--> ЧИТАТЬ ПОЛНОСТЬЮ <--