Курсовая работа: Оксикислоти
Багатоосновні оксикислоти можуть містити в молекулі дві, три і більше карбоксильних груп. Представниками дикарбонових оксикислот є оксі- і діоксіянтарні кислоти. Оксіянтарна, або яблучна, кислота вперше була виділена ще 1785 р. К. Шеєле з недостиглих яблук. Вона широко поширена в природі і міститься в кислих яблуках, горобині, аґрусі, барбарисі, махорці тощо. Яблучна кислота має один асиметричний атом вуглецю С*, виявляє оптичну активність і існує у вигляді (+) D - і (-) L-стереоізомерів (Тпл = 100 °С):

У природі поширена (-) L - яблучна кислота. Рацемічну яблучну кислоту (Тпл. =130 °С) можна добути гідратацією малеїнової кислоти або дією вологого оксиду срібла на рацемічну бром'янтарну кислоту:
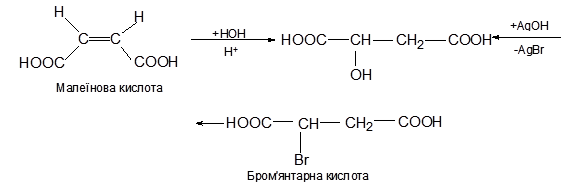
Діоксіянтарні кислоти називають винними. Вони містять два асиметричних атоми Кількість оптичних ізомерів, як уже зазнача
 |
??? ?????????? ?? ???????? 2п , ?? ? - ????? ???????????? ?????? ?*. ????, ??????????????? ?????????????? ?????? ??????? ???? ?????? (??? ??????? D-????, ??? - L-????), ????? ???? ??? ???????? ???????? ??????? ?????? ?? ?????? ????????. ? ??????? ???????, ? ????? ?????? ?????????? ???? ????? ???????: (+) - ????? (?), ?? ??????? (-) - ????? (II), ????????? (III) ? ??????? - (?) - ????? ???????, ??? ??????????? ???????????. ? ???????? ?????????? ??????? ?????? ??????????? ????? ?* ????????? ? ?????????? ????????? ? ???? ??? ????????? ????????. ???? ????, ? ?????????? ??????? ???????????? ????????? ??????????? ????????? ??????? ??????????? ?????? ?????????? ???????????? ????????????? ???????? ? ?????????? ?????????. ???? ????????? ??????? ? ??????? ?????????? ? ? ??? ????? ????????:
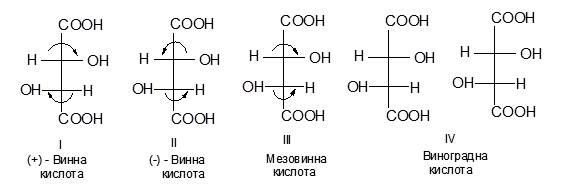
Причину оптичної неактивності мезовинної кислоти можна уяснити так. Припустимо, що розміщення Н, СООН і ОН біля асиметричного атома С* в такому порядку - від атома водню через карбоксил до гідроксилу за годинниковою стрілкою - зумовлює обертання площини поляризації світла вправо, а розміщення цих груп у протилежному порядку (проти годинникової стрілки) - обертання площини поляризації світла вліво. Після такого, припущення легко помітити, що в мезовинній кислоті Н, СООН і ОН біля верхнього атома С* розміщені за годинниковою стрілкою і повинні зумовлювати праве обертання, а біля нижнього атома С* ці самі групи розміщені проти годинникової стрілки і повинні зумовлювати ліве обертання. Оскільки групи біля верхнього і нижнього атомів С* однакові, то праве обертання верхньої частини молекули повинно повністю компенсуватися лівим обертанням нижньої частини молекули. В кінцевому результаті така винна кислота, хоч і мав асиметричні атоми С*, оптичної активності не виявляє.
(+) - " (-) - Винні кислоти є оптичними антиподами. Мезовинна кислота відносно цих винних кислот вже не е їх антиподом.
Такі стереоізомери, які не є антиподами, називають діастереоізомерами. Отже, (+) - винна і мезовинна, (-) - винна і мезовинна кислоти є діастереоізомерами. Діастереоізомери різняться між собою не тільки оптичним обертанням, але й іншими фізико-хімічними властивостями, тоді як у антиподів фізико-хімічні властивості однакові, а відмінні тільки напрямки обертання площини поляризації світла (див. табл.2).
Діастереоізомери утворюють також відмінні за властивостями похідні. Так, солі діастереоізомерних винних кислот значною мірою відрізняються за розчинністю у воді. Ця властивість має важливе практичне значення і використовується для розділення даних діастереоізомерів.
З винних кислот найбільше значення має (+) - винна кислота, яка називається D-винною, або виннокам'яною, кислотою.
Солі винної кислоти називають тартратами. Винна кислота і її солі містяться в багатьох плодах рослин, наприклад у винограді, горобині. Кисла калієва сіль винної кислоти важко розчиняється у воді. Вона міститься у виноградному соку і під час його переробки випадає в осад у вигляді "винного каменю".
Діючи на "винний камінь" мінеральною кислотою, можна добути (+) - винну кислоту:
![]()
Винну кислоту застосовують у харчовій промисловості, наприклад при виготовленні охолодних напоїв. Подвійна калій-натрієва сіль винної кислоти КООС-СНОН-СНОН-COONa відома під назвою сегнетової солі і використовується для виготовлення реактиву Фелінга, а також у радіотехніці (п'езокристали). Подвійна сіль калію і сурми 2С4 Н4 О6 К • (SbO) a • Н2 0 під назвою "рвотного каменю" застосовується в медицині, а також при протравному фарбуванні. Антипод виннокам'яної кислоти - (-) - винна кислота в природі не зустрічається. її можна добути з рацемічної (+) - винної (виноградної) кислоти розділенням кристалів на ліво - і правообертаючі ізомери. Виноградна, або (±) - винна, кислота є рацематом. Вона являє собою хімічну сполуку рівномолярних кількостей (+) - винної і (-) - винної кислот і тому не є оптично активною. У водному розчині виноградна кислота має мономерну, а не подвоєну молекулярну масу. Це свідчить про те, що при розчиненні рацемат дисоціює на (+) - і (-) - винні кислоти. Виноградну кислоту можна добути при тривалому нагріванні (+) - або (-) - винної кислоти, а також при окисленні фумарової кислоти водним розчином КМn04 :
 |
|
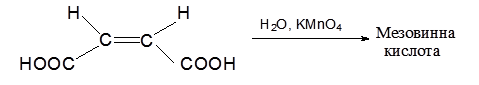
Під час кип'ятіння (+) - , (-) - винних або виноградної кислот з лугами, а також при окисленні малеїнової кислоти водним розчином КМn04 утворюється мезовинна кислота:
Представником трьохосновних оксикислот є лимонна кислота

Вона не містить асиметричного атома С* і тому є оптично неактивною. Лимонну кислоту вперше добув у 1784 р. Шеєле з лимонного соку, в якому її міститься 6÷10%. Ця кислота є також у смородині, малині, аґрусі, буряковому і виноградному соках, а у вигляді солей - в махорці, у невеликій кількості вона міститься в молоці і крові. Лимонна кислота відіграє важливу роль в процесах обміну речовин в живих організмах. У промисловості лимонну кислоту добувають лимоннокислим бродінням глюкози і патоки, а також з махорки після виділення з неї нікотину. Лимонна кислота використовується в харчовій промисловості при виготовленні кондитерських виробів, у медицині, текстильній промисловості при фарбуванні тканин тощо. Хлор'яблучні, або оксихлор'янтарні, кислоти належать до дикарбонових оксикислот з двома асиметричними атомами вуглецю:

Тому у хлор'янтарної кислоти існує 4 (22 = 4) оптичних ізомери, які зображуються проекційними формулами I-IV:

Речовини, в молекулах яких однакові замісники розміщені біля асиметричних атомів С* з одного боку, називають еритро-ізомерами; якщо ж ці замісники розміщені з різних боків, то їх називають трео-ізомерами. Крім стереоізомерів І-IV, існують дві рацемічні хлор'яблучні кислоти: рацемат (Тпл = 146 °С), який складається з (+) і (-) - еритро-форм і рацемат (Тпл =153 °С), який складається з (+) - і (-) - треоформ.
Суміш стереоізомерних хлоряблучних кислот можна добути приєднанням хлорнуватистої кислоти до малеїнової або фумарової кислоти:
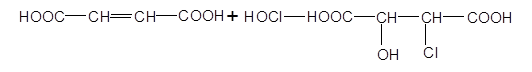
Оксикислоти в природі
Багато аліфатичних оксикислот мають природне походження й зустрічаються в різних рослинах, а також беруть участь в обмінних процесах живого організму. Так, гликолева кислота зустрічається в буряку й винограді, молочна кислота, як ми вже відзначали вище, є продуктом життєдіяльності деяких бактерій, наприклад, що забезпечують молочнокисле шумування молока й багатьох овочів при консервуванні, квашенні капусти й засолюванню огірків. Молочна кислота є природним консервантом, і її нагромадження охороняє продукти від подальшого розкладання. В організмі людини D-молочна кислота утвориться в м'язах при фізичному навантаженні в результаті розщеплення глюкози через стадію утворення найпростішої кетокислоти - пировиноградної кислоти, і її підвищена концентрація сприймається як м'язова утома.