Курсовая работа: Производство вольфрамового ангидрида вскрытием вольфрамового концентрата автоклавно–содовым выщелачиванием
где К—константа скорости реакции; К.с—константа равновесия; [Na2 CO3 и [Na2 WO4 ] - концентрации соды и вольфрамата натрия в объеме раствора. [1]
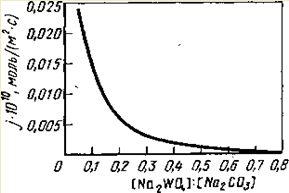
Рис. 1 Зависимость удельной скорости реакции разложения шеелита от молярного отношения концентрации Na2 WO4 /Na2 CO3 в растворе при 175 °С.
Как видно из рис.1, удельная скорость реакции уменьшается примерно обратно пропорционально возрастанию отношения молярных концентраций [Na2 WO4 ]: [Na2 СО3 ] в растворе, что соответствует уравнению c переменной I.
Это обусловливает необходимость применения значительного "кинетического" избытка соды. С целью снижения расхода соды проводят двустадийное противоточное выщелачивание: хвосты после первого выщелачивания, содержащие 15-20 % WOз от исходного количества, выщелачивают, используя большой избыток соды. Получаемый раствор, являющийся оборотным, поступает на первую стадию процесса. Однако расход соды и в этом случае не ниже 250 % от СНК.
Шеелитовые концентраты легче разлагаются растворами соды по сравнению с вольфрамитовыми. Добавление в автоклавную пульпу NaOH или СаО (что приводит к каустификации соды) позволяет снизить расход соды.
Содержание примесей в щелоках автоклавно-содового процесса определяется взаимодействием сопутствующих минералов с растворами соды при 200—225 °С. В растворах могут присутствовать примеси соединений Si, P, As, F, Mo, A1. Для окисления примеси молибденита (с целью извлечения молибдена в вольфраматный раствор), а также удаления примеси мышьяка применяют предварительный обжиг вольфрамовых концентратов при 650—700°С. Удаление флотореагентов в процессе обжига улучшает показатели автоклавно-содового разложения вследствие исключения вспенивания пульп. В таблице 2 приведены сопутствующие компоненты шеелитового концентрата, их форма нахождения в концентрате и характер взаимодействия с растворами соды при выщелачивании.
Таблица 2. Характер взаимодействия сопутствующих минералов шеелитовых концентратов с растворами соды при 200—225 °С
| Элемент | Минерал | Характер взаимодействия минерала с растворами соды | Соединение, пере-ходящее в раствор |
| Фосфор |
Апатит Са5 (Р04 )зF | Частично реагирует по обменной реакции с образованием фосфата и фторида натрия |
Na2 HPО4 ; (NaF) |
| Мышьяк |
Арсенопирит FeAsS Скородит FeAs04 |
Частично реагирует с образованием рас творимой тиосоли Реагирует с образованием арсената нагрия |
Na2 HAs04 Na2 HAs04 |
| Фтор | Флюорит CaF2 |
Частично реагирует По обменной реакции | NaF |
| Кремний и алюминий | Кварц, силикаты, алюмосиликаты |
Реагирует с образованием растворимых Силикатов и алюминатов натрия |
Na2 SiO3 , NaAl(OH)4 |
| Молибден |
Молибденит MoS2 ПовеллитСаМо04 |
К-во Просмотров: 693
Бесплатно скачать Курсовая работа: Производство вольфрамового ангидрида вскрытием вольфрамового концентрата автоклавно–содовым выщелачиванием
|