Курсовая работа: Специфичность фермента амилазы
Подобные ферменты называют синтазами.
Изомеразы.
Ферменты, относящиеся к этому немногочисленному (около 90 индивидуальных ферментов) классу, ускоряют геометрические или структурные изменения в пределах одной молекулы. Эти изменения могут состоять во внутримолекулярном переносе водорода, фосфатных и ацильных групп, в изменении пространственного расположения атомных группировок, в перемещении двойных связей и т.п. Важнейшими изомеразами являются триозофасфтизомераза, фосфоглицерат-фосфомутаза, альдозомутаротаза и изопентенилдифосфатизомераза.
Триозофасфтизомераза ускоряет перенос атомов Н в процессе превращения 3-фосфоглицеринового алдегида в фосфодиоксиацетон и обратно:
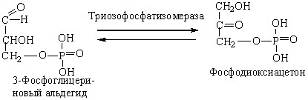
Фосфоглицерат-фосфомутаза обеспечивает достаточную скорость превращения 2-фосфоглицериновой кислоты в 3-фосфоглицериновую кислоту и обратно:

Мутароза является представителем стереоизомераз, она ускоряет реакцию превращения D-глюкопиранозы в D-глюкопиранозу:
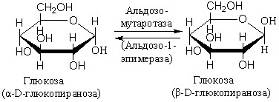
Изопентенилпирофосфат-изомераза катализирует реакцию перестройки изопентилпирофосфата в диметилаллилпирофосфат, что связано с перемещением двойной связи из 3-го во 2-е положение:
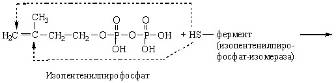
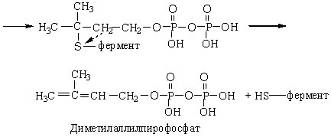
Изопентенилпирофосфат-изомераза содержит содержит свободные сульфгидридные группы, верятно, в виде радикала цис в белковой молекуле, и именно благодаря им обеспечивается указанная выше реакция, имеющая огромное значение для синтеза полизиопреноидов и стеролов.
Лигазы (синтетазы).
К лигазам относятся ферменты, катализирующие соединение друг с другом молекул, сопряженное с гидролизом пирофосфатной связи в молекуле АТФ или иного нуклеозидтрифосфата.
В качестве примера действия лигазы можно привести синтез пантотеновой кислоты из
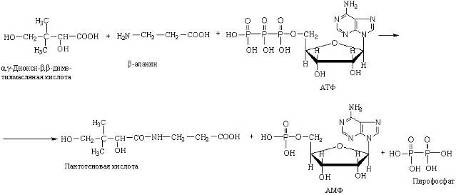
1.2 АМИЛАЗЫ. СТРОЕНИЕ, ФУНКЦИИ
Амилазы (от лат. amylum - крахмал), ферменты класса гидролаз, катализирующие гидролиз крахмала, гликогена и др. родственных олиго- и полисахаридов, гл. обр. по 1,4![]() глюкозидной связи (см., напр., схему в ст. О-Гликозидгидролазы). При приготовлении дрожжевого теста дрожжи разлагают крахмал с помощью амилазы до ди- и трисахаридов, которые потом используются в жизнедеятельности, образуя в результате спирт, углекислый газ (CO2 ) и другие метаболиты, которые придают хлебу специфический вкус и «поднимают» тесто. Однако, это длительный процесс, поэтому в современных технологиях амилаза используется как одно из важных составляющих специальной добавки, ускоряющий процесс брожения. Бактериальная амилаза используется в стиральных порошках для разложения крахмала, присутствующего в белье.
глюкозидной связи (см., напр., схему в ст. О-Гликозидгидролазы). При приготовлении дрожжевого теста дрожжи разлагают крахмал с помощью амилазы до ди- и трисахаридов, которые потом используются в жизнедеятельности, образуя в результате спирт, углекислый газ (CO2 ) и другие метаболиты, которые придают хлебу специфический вкус и «поднимают» тесто. Однако, это длительный процесс, поэтому в современных технологиях амилаза используется как одно из важных составляющих специальной добавки, ускоряющий процесс брожения. Бактериальная амилаза используется в стиральных порошках для разложения крахмала, присутствующего в белье.
![]() А. (мол. м. 50 тыс.) участвует в гидролизе сахаров, содержащих подряд три или более остатков глюкозы. Расщепление связей может происходить между любыми остатками глюкозы, причем остатки моносахаридов в месте разрыва имеют конфигурацию
А. (мол. м. 50 тыс.) участвует в гидролизе сахаров, содержащих подряд три или более остатков глюкозы. Расщепление связей может происходить между любыми остатками глюкозы, причем остатки моносахаридов в месте разрыва имеют конфигурацию![]() аномеров.
аномеров.![]() А. превращает амилозу крахмала в глюкозу и мальтозу. Находящийся в крахмале амилопектин, содержащий в молекуле 1,6
А. превращает амилозу крахмала в глюкозу и мальтозу. Находящийся в крахмале амилопектин, содержащий в молекуле 1,6![]() связи, полностью не гидролизуется - остается разветвленный полисахарид, т. наз. "остаточный декстрин".
связи, полностью не гидролизуется - остается разветвленный полисахарид, т. наз. "остаточный декстрин".![]() А. обладает слабокислыми св-вами. Ионы Са2+ и Cl- активируют ее. Присутствует во всех тканях животных и растений, а также в микроорганизмах. По каталитич. активности ферменты из разных источников значительно отличаются друг от друга.
А. обладает слабокислыми св-вами. Ионы Са2+ и Cl- активируют ее. Присутствует во всех тканях животных и растений, а также в микроорганизмах. По каталитич. активности ферменты из разных источников значительно отличаются друг от друга.![]() А. слюны, поджелудочной железы и слизистой кишечника участвуют в переваривании пищи,
А. слюны, поджелудочной железы и слизистой кишечника участвуют в переваривании пищи,![]() А. печени расщепляет гликоген.
А. печени расщепляет гликоген.
![]() А. (мол. м. 50-200 тыс.) последовательно отщепляет остатки
А. (мол. м. 50-200 тыс.) последовательно отщепляет остатки![]() мальтозы от невосстанавливающего конца цепи полисахаридов. Под действием
мальтозы от невосстанавливающего конца цепи полисахаридов. Под действием![]() А. из амилозы образуется мальтоза, а из амилопектина также "остаточный декстрин". Содержится
А. из амилозы образуется мальтоза, а из амилопектина также "остаточный декстрин". Содержится![]() А. в солоде.
А. в солоде.
![]() А. (экзо-1,4
А. (экзо-1,4![]() глюкозидаза; мол. м. 50-100 тыс.) последовательно отщепляет концевые остатки
глюкозидаза; мол. м. 50-100 тыс.) последовательно отщепляет концевые остатки![]() D-глюкозы от невосстанавливающих концов цепей полисахаридов с образованием
D-глюкозы от невосстанавливающих концов цепей полисахаридов с образованием![]() D-глюкозы. Способна также расщеплять 1,6
D-глюкозы. Способна также расщеплять 1,6![]() связь, если следующие за ней моносахариды соединены в положениях 1 и 4. Содержится в плесневых грибах. Определение активности А. используют в диагностич. целях, в частности для идентификации гликогеноза. А. (в т. ч. иммобилизованные) применяют в пром-сти:
связь, если следующие за ней моносахариды соединены в положениях 1 и 4. Содержится в плесневых грибах. Определение активности А. используют в диагностич. целях, в частности для идентификации гликогеноза. А. (в т. ч. иммобилизованные) применяют в пром-сти:![]() А.-для "осахаривания" крахмала,
А.-для "осахаривания" крахмала,![]() А.-для произ-ва глюкозы.
А.-для произ-ва глюкозы.
Функции. Амилаза - гидролитический фермент - разлагает крахмал и гликоген до мальтозы. Амилаза образуется преимущественно в слюнных железах и поджелудочной железе, поступает затем соответственно в полость рта или просвет двенадцатиперстной кишки и участвует в переваривании углеводов пищи. В сыворотке крови выделяют соответственно панкреатический и слюнной изоферменты амилазы. Значительно более низкой амилазной активностью обладают также такие органы как яичники, фаллопиевы трубы, тонкий и толстый кишечник и печень. Фермент выводится почками. Следовательно, увеличение сывороточной активности амилазы приводит к повышению активности амилазы в моче. Амилаза может образовывать крупные по размеру комплексы с иммуноглобулинами и другими белками плазмы, поэтому не проходит через почечные клубочки, поэтому содержание ее в сыворотке возрастает, в моче наблюдается нормальная активность амилазы.
Слюна содержит значительное количество амилазы — фермента, принимающего участие в переваривании углеводов, а также ферменты, расщепляющие белки. Все они активны только при щелочной или нейтральной реакции среды. Поэтому кислый желудочный сок прекращает их действие. Но, тем не менее, их влияние продолжается некоторое время в желудке, потому что пищевой комок не сразу пропитывается желудочным соком.
Слюна обладает бактерицидными (убивающими микробы) свойствами. Она предупреждает развитие кариеса зубов благодаря присутствию в ней фермента лизоцима. У человека слюноотделение связано и с речевой функцией: слюна обеспечивает во время речи увлажнение слизистой оболочки ротовой полости (установлено, что слюноотделение сопровождает даже акт письма). В течение суток выделяется от 0,5 л до 2 л слюны.
1.3 СПЕЦИФИЧНОСТЬ АМИЛАЗЫ
???????? ???????? ????? ??????? ??????????????. ??? ????????????? ??????????? ?????? ?????? ???????? ????????, ????? ??????????????? ????? ???????? ?????????. ??? ???????? ???????? ????????? ?????? ? ??????: ???????? ???????????? ? ??? ? ??????, ??????? ????? ???????? ? ?????, ?.?. ? ????????. ????? ?? ????????? ???? ???????? ??? ? 1959 ???? ????? ????????????? ???????? ?????? ? ?????? ????????? ???????. ?? ?????? ????? ? ???????? ???????? ??????? ?????????. ???????? ????? ?????????????, ???????? ?????????? ? ?????????, ???????? ????????? ? ????????? ??????????. ?????????? ????????? ? ???? ?????? ????? ??????? ????????, ??????? ??? ????????? ?? ???? ??????????????? ??????? ???????? ???? ?????.??????? ?????????? ????????????? ????? ????? ????? ???????: ?????? ???????????? ? ???? ??? ? ?????? ???????????? ????????? ?????. ????? ????????????????? ???????? ????? (???????? 20-30% - ??? ???????? ???????? ???????) ???????? ????????? ???? ?????????. ??????? ????? ???????????? ? ???????????? ????????? ????????? ??????, ?? ?????????? ??? ??? ???????????? ? ????? ????? 60%. ????? ?????? ???????? ???????????? ??????????; ???????????????? ????? ????????? ?????????? ? ???????? ?? 4,2 - 5,7. ???????????? ????? ????????? ??????? 60000, ?????? ???????????????? ?????? - 45000-50000. ?????? ?? ??????? ???????? ???? ? ???????????????, ???? ? ??????????????? ????. ???? ??????? ????????? ??????????????? ???????? ?? ???????. ??? ??????? ???? ?????????? ?????????????, ????? ???????????? ?????????. ? ????????? ????? ??? ??????? ???????? ????? ??? ???? ??????. ?????? ???????????? ???? ?????? ????????????? ? ????????????? ????????? ???????? ?? ??? ??? ?? ??????????.???????? ???????? ?????????:Амилаза действует на -1,4 -гликозидные связи, расщепляют амилозу внутри её цепи, в результате чего с большой скоростью образуются низкомолекулярные продукты гидролиза - нормальные декстрины. Их дальнейший гидролиз даёт мальтозу, мальтотриозу и глюкозу. Было найдено, что расщепление -1,4-глюкозидных связей в амилозе носит случайный характер иподчиняется закону статистического распределения продуктов реакции. Расщепление более мелких фракций на последнем этапе амилоза носит уже не случайный характер - действие фермента направлено лишь на определённые -1,4-гликозидные связи. В конечном счёте амилаза превращают амилозу в мальтозу и глюкозу, хотя и отмечены некоторые несущественные различия в динамике гидролиза этими ферментами указанного субстрата.
?????????, ???????? ?? ????????? ???????? ? ????????????????? ??????????? ???????????? ???????? ????????? ???????? (??????????????? ?????) ??????? Bac. Subtilis ?? ??????????? ???????. ?????? ????????? ???????????? ???????? ???????? ????????????????? ??????????? ??? ????????? ? ?????????????? ????????? ????????. ??? ???? ????????? ??????? ??????????, ??? ??? ????????? ????????? ?????????? ????????Амилазы специфичны у разных видов организмов. Физиологическая роль их состоит в мобилизации запасов полисахаридов в клетках (например, при прорастании семян). Велико значение их в процессе пищеварения: Амилазы содержатся в слюне и соке поджелудочной железы человека и животных. Так, амилаза расщепляет гликоген и крахмал до глюкозы и играет важную роль во внутриклеточном обмене гликогена. Микроорганизмы потребляют крахмал, выделяя в среду амилазу.
Определение активности амилазы в сыворотке крови и моче используется в диагностике заболеваний поджелудочной железы, печени, почек, слюнных желез, а также в диагностике гликогенозов.
1.4 ВЛИЯНИЕ ИНГИБИТОРОВ И АКТИВАТОРОВ НА АКТИВНОСТЬ АМИЛАЗЫ