Реферат: Молекулярна спектроскопія
де ![]() – момент кількості руху електрона по орбіталі,
– момент кількості руху електрона по орбіталі,
а – віддаль електрона від ядра,
me – маса електрона.
Обертова енергія молекули визначається за формулою:
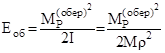 ,
,
де ![]() – обертовий момент кількості руху,
– обертовий момент кількості руху,
І – момент інерції,
М – приведена маса ядер,
ρ – розміри молекули.
![]() =
= ![]() ; а » ρ. Тоді
; а » ρ. Тоді ![]() .
.
Якщо виразити енергію в ккал/моль, то Еел ~ 100 ккал/моль, Екол ~ 1–10 ккал/моль, Еоб ~ 0,01–0,1 ккал/моль. Саме ця різниця в порядку Еел , Екол і Еоб приводить до того, що електронні, коливні і обертові спектри так різко відрізняються один від одного. Електронні спектри лежать в інтервалі частот від 10 000 см–1 і вище, коливні займають область примірно від 100 до 10 000 см–1 , а обертові – нижче 100 см–1 .
Обертовим спектрам відповідає випромінювання, що лежить в далекій інфрачервоній області оптичного спектра.
Коливним спектрам відповідають переходи, що лежать в ближній інфрачервоній області.
Електронним спектрам відповідає випромінювання, що лежать у видимій або ультрафіолетовій області.