Курсовая работа: Молибден
10.1. прогнозируйте отношение данного металла в компактном виде к атмосфере сухого воздуха (при комнатной температуре и нагревании), к влаге (без аэрации и при аэрации), к неокислительным и окислительным кислотам (на холоду и при нагревании), к растворам и расплавам щелочей.
10.2. Опишите процесс измерения стандартного электродного потенциала данного металла Cu и дайте термодинамический расчет этой величины.
10.3. Составьте и опишите схему гальванического элемента из металлического электрода данного металла и электродной системы С, ![]()
10.4. Опишите процесс электрохимической коррозии при контакте металла и изделия из Mg во влажной среде (Без аэрации и при аэрации). PH=10
10.5. Опишите процесс электролиза с учетом перенапряжения.
Электролит – раствор ![]() PH= 4, 5
PH= 4, 5
Электроды: катод – Сu,
анод – Zn.
11. Применение.
РЕШЕНИЕ
4. Электронное строение атома.
4.1. Составьте электронную формулу данного элемента.
Порядковый номер элемента в периодической системе химических элементов Д. И. Менделеева равен 42. Это значит, в молекуле молибдена будет 42 электрона.
Электронная формула молибдена будет такова: ![]()
Составим также его электронно – графическую формулу:
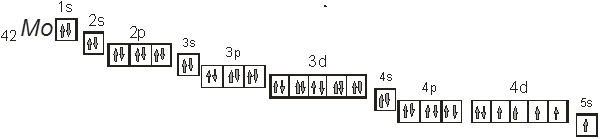
На рисунке выше приведена электронно – графическая формула молибдена.
4.2. Дайте объяснение физического смысла всех индексов у данного химического элемента в системеД.И. Менделеева (порядковый номер, номер периода, номер группы, принадлежность к группе «А» или «Б»). Определите возможность «Эффекта провала электрона».
Порядковый номер химического элемента в периодической системе химических элементов – 42. у молибдена на электронных уровнях находится 42 электрона, а в ядре должно находится также 42 протона.
Молибден расположен в периодической системе химических элементов в пятом периоде, это значит, что у него будет пять электронных слоев с расположенными на них электронами. Главное квантовое число внешнего электронного уровня равно 5.
Молибден расположен в шестой группе, побочной подгруппе. Молибден относят к элементам подгруппы хрома , в которую входят хром, молибден и вольфрам, которые обладают похожими свойствами. У него будет на электронных уровнях один s-электрон и 5 d-электронов на пред внешнем уровне.
В состав ядра атома изотопа молибдена-96 входят 42 протона (p) и 54 нейтрона (n): ![]() , где массовое число и порядковый номер элемента (число протонов) обозначают числовыми индексами слева от символа химического элемента; верхний индекс означает массовое число, нижний – заряд ядра. Количество нейтронов ядра элементов определяют по массовому числу элемента за вычетом количества протонов.
, где массовое число и порядковый номер элемента (число протонов) обозначают числовыми индексами слева от символа химического элемента; верхний индекс означает массовое число, нижний – заряд ядра. Количество нейтронов ядра элементов определяют по массовому числу элемента за вычетом количества протонов.
Таким образом, в состав атома молибдена входят ядро, состоящее из 42 протонов, 54 нейтронов и электронное облако, представленное 42 электронами.
Вследствие устойчивости d5 -конфигурации энергетически оказывается более выгодным переход одного из ns-электронов в (n-1) d-состояние. Поэтому молибден, как и хром в s-состоянии внешнего уровня имеют по одному, а в предпоследнем слое по 13 электронов. Таким образом, имеет место «проскок» электрона:
![]()
Проскок электрона можно объяснить с точки зрения квантово-механических представлений повышенной энергетической стабильностью конфигурации: 4d5 .
4.3. Выделите валентные подуровни в электронной формуле атома химического элемента, определитепринадлежность химического элемента к типу s-, p-, d-, f-элементов.
Покажем расположение валентных электронов в атоме молибдена. Как видно из электронной формулы моилбден относится к d-элементам, поскольку у него заполняется 4d-подуровень.

![]()