Курсовая работа: Редкоземельные металлы и их полуторные оксиды
C – Dy2O3
350, 450, 500
600, 1000
500, 600
700, 850, 1000, 1100
600, 700, 775
850, 1000, 1200
500, 1000, 1100
1200, 1300, 1400
500, 900, 1000, 1300
1400
500, 1000, 1300, 1500
500, 1000, 1400
500, 1000, 1400
В работах различных авторов было подвергнуто проверке положение Гольдшмидта об обратимости фазовых превращений в оксидах РЗЭ при изменении температуры. Яндели [8], Вольф и Бернигхаузен [7] не могли установить, несмотря на многочисленные повторения и длительные выдержки, ни в одном случае обратимого перехода модификаций С и А.
Выяснить устойчивость оксидов и гидрооксидов редкоземельных элементов пытались Шафер и Рой [6], изучая фазовые равновесия в системах оксид редкоземельного элемента—вода. Учитывая, что при низком парциальном давлении паров воды энергия активации образования новой структуры из структуры, полученной при высоких температурах, очень велика, что может проявиться в образовании аморфных или метастабильных фаз, а также в получении неправильных значений равновесных температур фазовых превращении, Шафер и Рой проводили свои опыты при высоком давлении водяных паров. Схема полиморфных превращений, по их данным, показана на рис. 3.
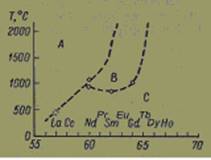
Рис. 3. Диаграмма фазовых превращений, по данным Шафера и Роя [6].
Следует, однако, помнить, что эти данные получены при равновесных и близким в к равновесным условиях и не могут быть сравнимы с результатами, полученными другими методами.
В работе Рота и Шнайдера [4] собран обширный материал об оксидах редкоземельных элементов, проведена ревизия предположений Гольдшмидта о механизме полиморфизма, а также подвергнуты сомнению выводы Лоберга, Роя и Шафера о существовании обратимых полиморфных превращений в рассматриваемых оксидах.
При проведении исследований Рот и Шнайдер использовали реактивы, содержащие 99.9% основного соединения, за исключением оксалата самария, в котором присутствовал 1% Еu, и окиси неодима, содержавшей около 2% различных примесей. До температуры опыта 1650° образцы помещали в печь в платиновом тигле (или подвешивали на платиновой проволоке), при температуре выше 1650° — в иридиевом тигле. После обжига образцы закаляли и подвергали рентгеновскому анализу при комнатной температуре. Отдельные опыты были проведены в вакууме (с оксидами церия и празеодима) и в гидротермальных условиях (с оксидом неодима).
Области устойчивости различных кристаллических форм, полученные в данной работе, приведены на рис. 4, из которого следует, что А-тип структуры оксидов редкоземельных элементов устойчив для больших ионов, В-тип — для промежуточных и С-тип — для малых ионов. Кроме этого, было установлено, что С-тип может встречаться как метастабильная форма при низких температурах для всех А- и В-типов оксидов.
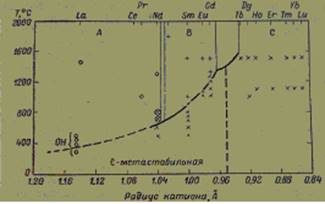
Рис. 4. Диаграмма фазовых превращений, по данным Рота и Шнайдера [4]
Гольдшмидт считал, что переходы из одного типа структуры в другой для оксидов редкоземельных элементов энантиотропны. Рот и Шнайдер не обнаружили никаких энантиотропных переходов. Они установили, что оксид неодима образует С-тип структуры при низких температурах и превращается необратимо в А-тип около 650°, оксиды Sm2 O3 , Еu2 O3 и Gd2 O3 также кристаллизуются при низких температурах в С-типе и превращаются непосредственно и необратимо в В-тип структуры при 950, 1075 ц 1225° соответственно.
Шафер и Рой делают вывод, что превращения в оксидах редкоземельных элементов представляют собой «полностью обратимые полиморфные превращения».
В-тип как стабильная кристаллическая фаза получен у оксидов самария, европия и гадолиния. Кроме этого, как показали Шнайдер и Рот [4], В-тип структуры часто встречается в бинарных системах оксидов редкоземельных элементов (например, в системах оксида неодима с оксидами самария, европия, гадолиния, диспрозия, гольмия, эрбия, тербия, иттербия и лютеция). Следовательно, введение или присутствие примесей в оксиде неодима может повысить устойчивость В-модификации.
Таким образом, если Гольдшмидт считал, что оксиды редкоземельных элементов кристаллизуются в трех типах структуры (А. В, С), устойчивость которых определяется температурой опыта с размером ионов РЗЭ, Шнайдер и Рот рассматривают только влияние размера иона. Они считают, что А-форма характерна для больших, В — промежуточных и С — малых катионов. Такая точна зрения основывается на том, что переходы С в А и С в В в этих оксидах необратимы и, возможно, монотропны, следовательно, С модификации дли больших катионов не может рассматриваться как устойчивая фаза для этих оксидов.
В 1961 г. появилась работа Уоршау и Роя [5], целью которой была проверка и уточнение результатов, полученных как Шафером и Роем, так и Шнайдером и Ротом. Для экспериментов использовались закалочные печи сопротивления с нагревателем из Рt+40% Rh (до 1850°) и из иридия (до 2400°). При температурах ниже 1000° часто использовались гидротермальные условия, так как при этом увеличивается диффузия ионов, что приводит к более быстрому установлению равновесия. Во время опытов исследуемый образец находился в контакте с водой только при самой высокой температуре опыта: вода вводилась в автоклав после достижения нужной температуры и удалялась до быстрого охлаждения автоклава. После удаления паров воды образцы сушили при температуре опыта от получаса до 3 часов, после чего охлаждали быстро до комнатной температуры. В данной работе было обращено также внимание на чистоту реактивов: исследуемые оксиды содержали не более 0.1—0.2% примесей. Для определения равновесной температуры перехода одной формы в другую нагревали одновременно обе формы, после чего определяли изменения в каждой из них.