Реферат: Начала термодинамики
Другая формулировка II-го начала, также являющаяся обобщением экспериментальных данных, была введена Клаузиусом в 1850г.: “Тепло не может самопроизвольно перейти от менее нагретого тела к более нагретому”. Положим, что эта формулировка эквивалентна более поздней формулировке Клаузиуса о существовании функции состояния энтропии.
Пусть имеется некоторая система, состоящая из двух термостатов с температурами ![]() , между которыми проходит теплообмен.
, между которыми проходит теплообмен. ![]() – количество тепла, отдаваемое термостатом с меньшей температурой, а
– количество тепла, отдаваемое термостатом с меньшей температурой, а ![]() – количество тепла, получаемое термостатом с большей температурой.
– количество тепла, получаемое термостатом с большей температурой.
Поскольку процесс совершается самопроизвольно, то суммарнаяработа, совершаемая за цикл должна быть равна нулю. Это возможно только в том случае, если адиабаты 2-3 и 4-1 пересекаются. Тогда
![]() ,
, ![]() ,
, ![]() ,
,
т.е., в принципе было бы возможным “подстроить” характеристики процесса таким образом, чтобы
![]() .
.
Однако совершить такой процесс не представляется возможным, поскольку, как уже было показано, адиабата (изоэнтропа) соответствует однозначной функцией состояния и, соответственно, пересечение адиабаты невозможно.
С положением о непересечении адиабат связана еще одна формулировка II-го начала термодинамики, предложенная в 1909 г. Каратеодори и признаваемая многими авторами наиболее удачной: вблизи каждого термодинамического состояния всегда есть состояние, перейти в которое посредством квазистатического адиабатического процесса невозможно.
Например, не существует адиабат, переводящих систему из состояния 2 через состояние 3 в состояние 1 (рис.3) или адиабат 4- Д, 1-Д, 3-С, 2-С на рис. 4.
Введенный принцип получил название принципа адиабатической недостижимости Каратеодори. Наглядно его можно проиллюстрировать с помощью семейства непересекающихся поверхностей с фиксированными значениями энтропии термодинамической системы.
Далее воспользуемся II-м началом термодинамики для уточнения калорического эффекта термодинамического процесса (2.5). Запишем:
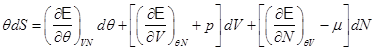 . (2.16)
. (2.16)
Выражение (2.16) и подобные ему, некоторые авторы называют обобщенной формулировкой I и II начала термодинамики.
Преобразуем дифференциал ![]() , и подставим его в (2.5):
, и подставим его в (2.5):
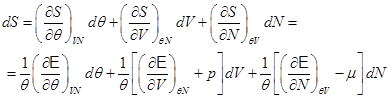 .
.
Из последнего равенства следует:
![]() ,
, 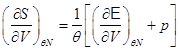 ,
, 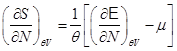 .
.
(2.17)
Учитывая, что
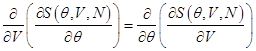 ,
,
получаем
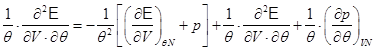 .
.
Выполняя преобразования в последнем равенстве, имеем:
![]() . (2.18)
. (2.18)
Аналогичным образом, учитывая
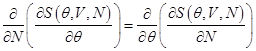 ,
,
Находим:
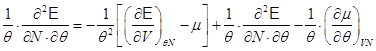 .
.
Последнее выражение можно переписать в виде: