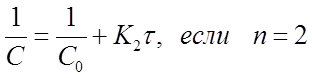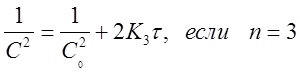Реферат: Скорость образования, расходования компонента и скорость реакции
Рассмотрим сначала исходные формулы.
Пусть зависимость скорости реакции (22) по первому исходному веществу А1 выражается уравнением (при условии, что остальные вещества в избытке):
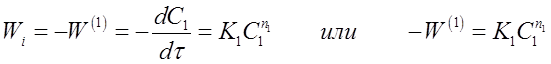
где п1 - порядок реакции по первому веществу.
Прологарифмируем полученное выражение:
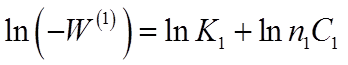 (28)
(28)
Так как скорость реакции по исходному веществу является отрицательной величиной, то значение 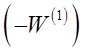 положительно. На графике в координатах
положительно. На графике в координатах 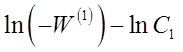 опытные точки для разных моментов времени, в случае справедливости уравнения (28) должны расположиться на прямой линии (рисунок 6). Отрезок на оси ординат дает значение ln К1 , а тангенс угла наклона а прямой линии равен порядку п1 по первому веществу.
опытные точки для разных моментов времени, в случае справедливости уравнения (28) должны расположиться на прямой линии (рисунок 6). Отрезок на оси ординат дает значение ln К1 , а тангенс угла наклона а прямой линии равен порядку п1 по первому веществу.
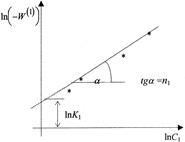
Рисунок 6 - Графическое определение порядка реакции по веществу
Скорость изменения концентрации вещества определяется непосредственно из эксперимента или из кинетической кривой (рисунок 5).
Есть и другие дифференциальные способы. Их достоинство -простота. Недостаток - большая погрешность в определении tga из
графика. Более точные результаты дают интегральные способы.
1.5.3 Интегральные способы
В этих способах используют выражения для зависимости концентрации веществ от времени (уравнения кинетических кривых), полученные после интегрирования уравнений вида:
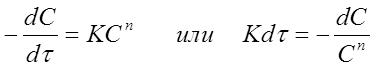 (29)
(29)
Рассмотрим некоторые интегральные способы.
1. Способ подстановки
Проинтегрируем уравнение (29) в пределах от 0 до τи от С0 до С при п = 1, 2, 3, при этом получим:
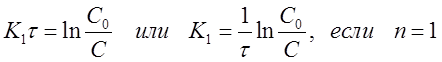 (30)
(30)
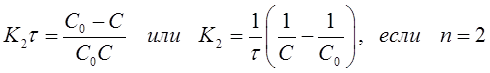 (31)
(31)
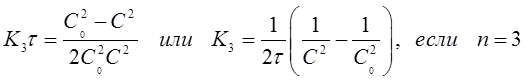 (32)
(32)
где C 0 - начальная концентрация исходного вещества.
Подстановкой в эти уравнения опытных значений концентраций С исследуемого вещества, в разные моменты времени протекания реакции, вычисляют значения К. Если расчетные К, например, по уравнению (31) остаются постоянными, то это означает, что порядок реакции по веществу равен двум.
В способе подстановки для реакций 2го порядка, когда концентрации исходных веществ неравны можно использовать формулу (16).
2. Графический способ
Перепишем уравнения (30)...(32) в виде:
![]()