Реферат: Зонная теория твердых тел
Cos k′a может меняться в пределах от –1 до +1.
Провели параллельные прямые оси абсцисс и находим точки пересечения этих прямых с графиком, опускаем перпендикуляры и находим корни уравнения (3). Эти участки обозначены жирными линиями. Таким образом допустимые значения Е(к) имеют дискретный характер (зонный). Если ось (Ка) перевернуть в вертикальное положение, то получим картину расположения энергетических зон, разрешенных и запрещенных.
 |
???.4
На рис.4 энергетический спектр электронов в кристалле имеет зонную структуру.
L – длина кольца цепочки.
Значения волновых векторов ![]() . α - постоянная решетки.
. α - постоянная решетки.
Зону, произошедшую от валентных уровней атомов, образующих кристалл, называют валентной зоной.
Зоны, произошедшие от внутренних уровней, всегда полностью заполнены электронами.
Частично заполненной или незаполненной может быть внешний валентный уровень (зона проводимости).
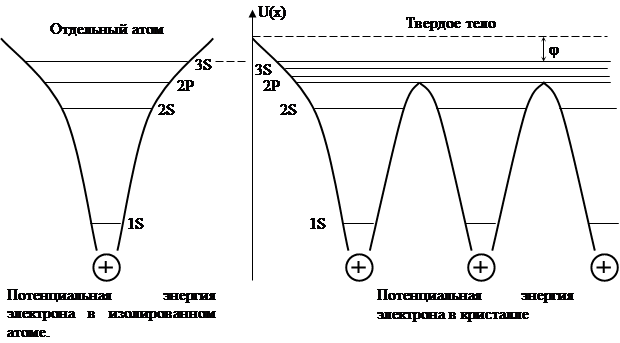
Рис.5 Рис.6
Наиболее слабо связаны 3S-электроны. При образовании твердого тела из отдельных атомов происходит перекрытие волновых функций этих электронов.
![]()
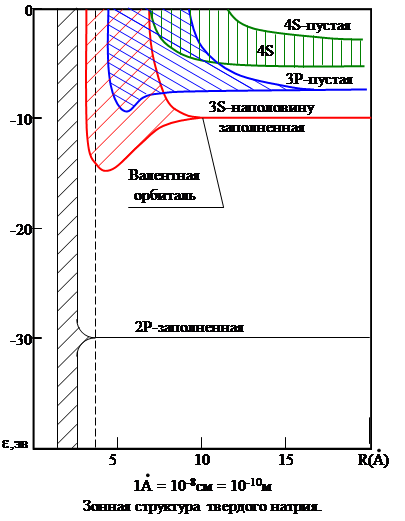 Пространственная протяженность электронных волновых функций зависит от квантовых чисел. Для больших квантовых чисел электронные волновые функции простираются на большие расстояния от ядра, для этих уровней взаимное влияние атомов будет проявляться при больших расстояниях между атомами. Что хорошо видно на рис.7, на примере уровней атомов натрия. На уровнях 1S, 2S, 2P практически не сказывается влияние соседних атомов, тогда как для уровней 3S, 3P и более высоких уровней это влияние существенно и эти уровни превращаются в энергетические зоны. Для 3S – электронов имеется энергетический минимум, обеспечивающий устойчивую твердотельную конфигурацию атомов натрия при средней межатомной расстоянии R~ 3А. В атоме натрия на энергии 3S – электрона сказывается влияние соседних атомов, означает также заметное перекрытие волновых функций этих электронов. Поэтому уже нельзя говорить о том, что конкретный 3S – электрон связан с каким-то конкретным атомом. Когда присутствие других атомов изменяет потенциальную яму отдельного атома (рис.5, рис.6), результирующий кулоновский потенциал уже не будет удерживать 3S – электроны около конкретных атомов, так что они могут находиться в твердом теле где угодно в результате перекрытия волновых функций 3S – электронов. Но 3S – электроны не могут свободно покидать твердое тело, так как их волновые функции не «выходят» за пределы вещества. Энергия связи электронов в твердом теле равна работе выхода φ.
Пространственная протяженность электронных волновых функций зависит от квантовых чисел. Для больших квантовых чисел электронные волновые функции простираются на большие расстояния от ядра, для этих уровней взаимное влияние атомов будет проявляться при больших расстояниях между атомами. Что хорошо видно на рис.7, на примере уровней атомов натрия. На уровнях 1S, 2S, 2P практически не сказывается влияние соседних атомов, тогда как для уровней 3S, 3P и более высоких уровней это влияние существенно и эти уровни превращаются в энергетические зоны. Для 3S – электронов имеется энергетический минимум, обеспечивающий устойчивую твердотельную конфигурацию атомов натрия при средней межатомной расстоянии R~ 3А. В атоме натрия на энергии 3S – электрона сказывается влияние соседних атомов, означает также заметное перекрытие волновых функций этих электронов. Поэтому уже нельзя говорить о том, что конкретный 3S – электрон связан с каким-то конкретным атомом. Когда присутствие других атомов изменяет потенциальную яму отдельного атома (рис.5, рис.6), результирующий кулоновский потенциал уже не будет удерживать 3S – электроны около конкретных атомов, так что они могут находиться в твердом теле где угодно в результате перекрытия волновых функций 3S – электронов. Но 3S – электроны не могут свободно покидать твердое тело, так как их волновые функции не «выходят» за пределы вещества. Энергия связи электронов в твердом теле равна работе выхода φ.
Твердое тело из четырех атомов будет иметь всего четыре уровня, распределенные по некоторому энергетическому интервалу.
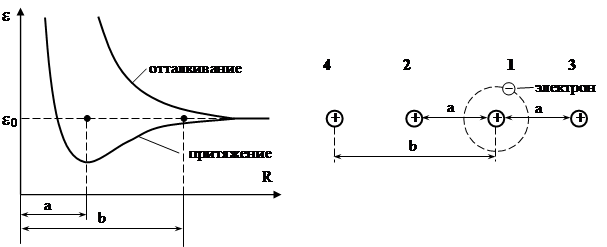
Рис.8
Например: в основном состоянии атома водорода электрон может находиться в одном из двух состояний – со спином вверх или вниз. В системе четырех протонов имеется восемь возможных состояний. Но если добавить еще три электрона, чтобы получить четыре атома водорода, то занятыми окажутся четыре состояния и на каждый электрон будет приходиться по два состояния. Эффект сближения атомов проявляется в изменении энергии отдельных состояний
![]()
где ![]() - энергия изолированного атома,
- энергия изолированного атома, ![]() - изменения энергии, связанные с влиянием соответствующих протонов 2, 3, 4. R – расстояние между атомами.
- изменения энергии, связанные с влиянием соответствующих протонов 2, 3, 4. R – расстояние между атомами.
Эффект сближения атомов проявляется в увеличении общего числа уровней. В реальном теле содержится порядка 1023 отдельных уровней, которые непрерывно распределяются внутри некоторого интервала, образуя зону разрешенных значений энергии (рис.9). Такая же ситуация в основном имеет место для валентных электронов любого атома.
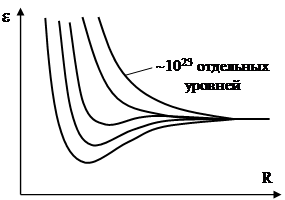 |
???.9
В твердом натрии зона 3S – электронов является внешней, наполовину заполненной. Верхняя граница заполненных уровней приходится на середину зоны. Электрон может перейти на более высокий свободный уровень в этой зоне за счет теплового или электрического возбуждения. Следовательно, твердый натрий обладает хорошей электропроводностью и теплопроводностью. На рис.10 зонная структура проводников (натрия). Верхняя зона – частично заполненная зона. Нижние зоны - заполненные электронами.
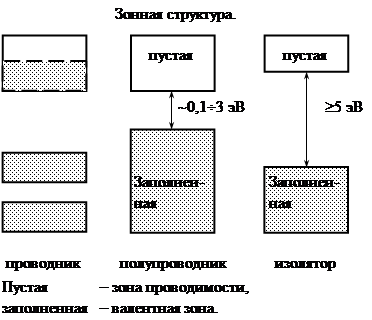
 Если число энергетических уровней в зоне больше числа электронов в ней, то электроны легко возбуждаются, обеспечивая тем самым проводимость, если же все уровни в зоне заполнены, то проводимость невозможна или затруднена.
Если число энергетических уровней в зоне больше числа электронов в ней, то электроны легко возбуждаются, обеспечивая тем самым проводимость, если же все уровни в зоне заполнены, то проводимость невозможна или затруднена.
![]() Например: в кремнии, германии, углероде (алмаз) на P – оболочке имеются два электрона и возникает смешанная конфигурация S и P – орбиталей (орбиталь – волновая функция, описывающая данное квантовое состояние), которая делает особенно благоприятной конфигурацию из четырех атомов, изображенную на рис.11 (энергия кулоновского отталкивания электронов минимальна).
Например: в кремнии, германии, углероде (алмаз) на P – оболочке имеются два электрона и возникает смешанная конфигурация S и P – орбиталей (орбиталь – волновая функция, описывающая данное квантовое состояние), которая делает особенно благоприятной конфигурацию из четырех атомов, изображенную на рис.11 (энергия кулоновского отталкивания электронов минимальна).
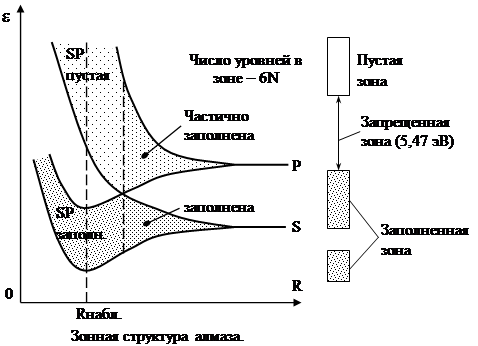
Рис.11
Волновые функции S и P – электронов образуют одну совершенно пустую гибридную SP – зону и одну заполненную гибридную SP – зону. Заполненная и пустая зоны разделены довольно значительным энергетическим интервалом или зоной запрещенных значений энергии. Для изоляторов типичное значение ширины запрещенной зоны ~ 5 эв и больше. Ширина запрещенной зоны для полупроводников (германия 0,67 эв, кремния 1,12 эв) находится в пределах 0,1 ¸ 3 эв.
Полупроводники и изоляторы отличаются друг от друга только шириной запрещенной зоны.
Рис.12
 |
§ Теорема Блоха
Теорема Блоха утверждает, что собственные функции волнового уравнения с периодическим потенциалом имеют вид произведения функции плоской волны
![]()
На функцию ![]() , которая является периодической функцией в кристаллической решетке:
, которая является периодической функцией в кристаллической решетке:
![]()