Учебное пособие: Изучение некоторых вопросов термодинамики
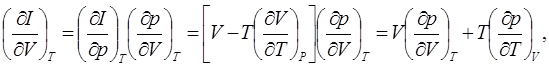 (7.10)
(7.10)
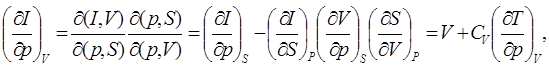 (7.11)
(7.11)
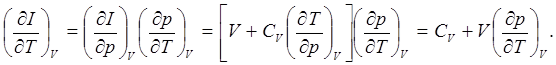 (7.12)
(7.12)
Однако это значение частной производной можно определить и более простым способом, если учесть, что I=U+pV и dI=dU+d(pV). Тогда

Важно подчеркнуть, что одно и то же значение частной производной, при постоянном значении выбранного параметра, можно получить несколькими способами в зависимости от выбора промежуточных переменных. Учитывая это, при решении задач, можно ввести такие якобианы, тождественно равные единице, которые относительно быстро приведут к цели. Покажем это на одном примере.
a)  (7.13)
(7.13)
где были использованы (3.1) и (2.2).
b)  (7.14)
(7.14)
Аналогичное значение, но с помощью введения переменных S и p было получено ранее в выражении (6.9).
Приведённый пример показывает, что для проверки правильности нахождения одной и той же термодинамической величины можно использовать несколько вариантов, хотя и в данном примере использованы не все.
СПОСОБЫ ОПРЕДЕЛЕНИЯ CP ДЛЯ ИДЕАЛЬНОГО ГАЗА.
Из объединённого выражения обоих начал термодинамики следует, что если подвод теплоты к системе осуществляется при изобарическом процессе, то TdS=CP dT, или
Однако, теплоемкость Cp для идеального газа можно определить как частную производную от тепловой функции по температуре. Действительно, при изобарическом процессе
 (8.1)
(8.1)
Это соотношение нетрудно понять, поскольку при р=const
dI=TdS+Vdp=TdS=Cp dT.
Найдём связь между изменениями температуры и тепловой функции при изохорическом процессе.
 (8.2)
(8.2)
где учтено выражение (7.11).
В случае адиабатического процесса изменения тех же величин дают:
 (8.3)
(8.3)
где использованы соотношения (2.2), (2.8), (7.10) и (8.2).
Непосредственной проверкой нетрудно убедиться, что для идеального газа
 (8.4)
(8.4)
Читателям представляется возможность найти удовлетворительное, с точки зрения законов термодинамики, объяснение выражений (8.4).
По аналогии с вышеприведенными примерами, можно решить большое количество задач, связанных со свободной энергией, энтальпией и термодинамическим потенциалом Гиббса.
Вышеприведенные примеры убедительно доказывают преимущество такого подхода к решению задач термодинамики. Этим способом, в основном, решаются и задачи, связанные с термодинамикой стержней, диэлектриков и магнетиков, примеры которых приведены в [4] и [7], для которых можно учесть электро- и магнитострикционные явления, пьезоэлектрический и пьезомагнитный эффекты, а также и задачи, связанные с химическим потенциалом, когда количество вещества в системе изменяется .
Применение якобианов, особенно после изучения свойств термодинамических функций и их дифференциалов, позволяет более доступным способом решить ту или иную задачу, и, что очень важно, даёт возможность, даже при решении одной задачи, охватывать большой материал, предусмотренный программой. Преимущество такого подхода к рассмотрению отдельных, или группы, вопросов, как показали наши наблюдения, не вызывает сомнений как с точки зрения корректности математических выражений, так и логичности и взаимосвязи явлений термодинамики.
СОСТАВЛЕНИЕ ДЕТЕРМИНАНТОВ ЯКОБИ И ТАБЛИЦЫ ТЕРМОДИНАМИЧЕСКИХ КОЭФФИЦИЕНТОВ ДЛЯ СИСТЕМ, ОПИСЫВАЕМЫХ БОЛЬШИМ ЧИСЛОМ ПЕРЕМЕННЫХ.
В качестве примера рассмотрим систему, описываемую тремя независимыми переменными, например, систему с переменным количеством вещества. В этом случае дифференциалы термодинамических функций имеют вид:
dU=TdS-pdV+mdN, (9.1)