Дипломная работа: Качественный анализ (кислотно-основная классификация)
Ва2+ + СгО4 2 - = Ва СгО 4 (желтый кристаллический)
2 Ва2+ + Сг,О7 2 - + 2 СН3 СОО- + НОН = 2 ВаСгО4 + 2 CH3 COOН
Растворяется в сильн. кислотах (кроме H2 SO4 ), не растворяется в уксусной кислоте.
5. Окрашивание пламени горелки.
Соли и другие соединения бария окрашивают бесцветное пламя горелки в желто-зеленый цвет.
Аналитические реакции катионов IV аналитической группы по кислотно-основной классификации: Zn2+ , Al3+ , Sn2+ , Sn4+ , As3+ , As5+ , Cr3+
Групповой реагент - гидроксид натрия или калия в присутствии Н2 О2
Аналитические реакции катиона цинка Zn2+
1. Реакция с щелочами:
Zn2+ + 2 ОН- = Zn(OH)2 (белый)
Zn(OH)2 + 2 ОН- =• [Zn(OH)4 ]2 - (бесцветный)
2. Реакция с раствором аммиака:
Zn2+ + 2 NH3 -H2 O —► Zn(OH)2 (белый) + 2 NH4 + Zn(OH)2 + 4 NH3 — [Zn(NH3 )4 ] (OH)2 (бесцветный)
Осадок нерастворим в разбавленной НС1, растворяется в щелочах.
3. Реакции с сульфид-ионами (фармакопейная):
Zn2+ + S2- = Zn S (белый)
Реакцию часто проводят в уксусной среде.
4. Реакция с гексацианоферратом (II) калия (фармакопейная)
Реакцию проводят в нейтральной или слабокислой среде, при нагревании
2 К+ + 3 Zn2+ + [Fe(CN)6 ]4- = К2 Zn3 [Fe(CN)6 ]2 (белый)
Осадок нерастворим в разбавленной НСl, растворяется в щелочах
5. Реакция с литизоном (дифенилтиокарбазоном). В растворах дитизона
устанавливается таутомерное равновесие между тионной и тиольной формами:
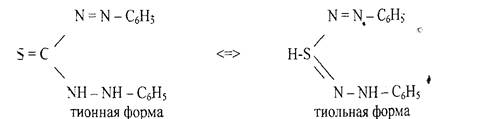
В результате реакции с катионами цинка возникает внутрикомплексное соединение, содержащее два дитизонатных аниона:
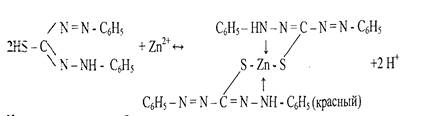
Наличие щелочи способствует смещению равновесия вправо вследствие связывания выделяющихся ионов водорода в молекуле воды. 6. Реакция образования -зелени Ринмана-.
Zn(NO3 )2 + Co(N03 )2 —t-> CoZn02 (зеленый) + 4 NO2 +О2 .
-Зелень Ринмана- - смешанный оксид кобальта и цинка CoZnO2 зеленого цвета.
Другие реакции катионов цинка.
Катионы Zn2+ при взаимодействии с различными другими реактивами образуют осадки: с Na2 HPO4 - белый Zn3 (PO4 )2 (растворяется в кислотах и в аммиаке); с К2 Сг04 -желтый ZnCrO4 (растворяется в кислотах и щелочах); с СоС12 и (NH4 )2 [Hg (SCN)4 ] -голубой ZnCo[Hg (SCN)4 ]; а также с различными орг. реагентами.
Аналитические реакции катиона алюминия Al3+
1. Реакция с щелочами: