Дипломная работа: Качественный анализ (кислотно-основная классификация)
А1(ОН)3 + 3 ОН- -> [А1(ОН)6 ]3 -
После растворения гидроксида алюминия и образования гидроксокомплексов алюминия к раствору прибавляют несколько кристаллов соли аммония (NH4 C1). Смесь нагревают. Гидроксокомплексы разрушаются выпадает осадок А1(ОН)3 :
[А1(ОН)6 ]3 - + 3 NH4 + -> А1(ОН)3 + 3 NH3 + 3 Н2 О
Наиболее полное осаждение гидроксида алюминия происходит при рН- 5-6. Осадок А1(ОН)3 растворяется в кислотах, но не растворяется в аммиаке.
2. Реакция с аммиаком.
А13+ + 3 NHr H2 O -> А1(ОН)3 1 (белый аморфный) + 3 NH4 +
3. Реакция с нитратом кобальта - образование -тенаровой сини- (фармакопейная).
-Тенаровая синь- - смешанный оксид алюминия и кобальта синего цвета.
2 A12 (SO4 )3 + 2 Co(NO3 )2 —tT-> 2 Со(А1О2 )2 + 4 NO2 + 6 SO3 + O2 .
4. Реакция с алюминоном
Катионы А13+ при взаимодействии с алюминоном – аммонийной солью ауринтрикарбоновой кислоты (для кратности NH4 L) образуют в уксуснокислой или аммиачной среде комплекс красного цвета (по-видимому, состав A1(ОН)2 L. Точное строение комплекса неизвестно. Выпадает красный хлопьевидный осадок. Мешают катионы Са2+ , Cr3+ , Fe3+
5. Реакция с ализарином (1,2 - диоксиантрахинон).
Катионы А13+ с ализарином и его производными в аммиачной среде образует комплексы ярко красного цвета называемые -алюминиевыми лаками-.
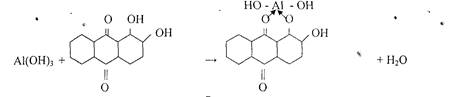
Комплекс устойчив в уксусной среде. Реакция высокочувствительна: предел обнаружения 0,5 мкг. Мешают катионы: Zn2+ , Sn(II), Cr3+ , Mn2 +, Fe3+ и др.
Другие реакции катиона алюминия А13+ .
Катионы А13+ образуют также осадки при реакциях в растворах: с Na2 HPO4 - белый А13 РО4 , с CH3 COONa- белый СН3 СООА1(ОН)2 , с оксихинолином (кратко Нох ) - желто-зеленый [А1(О)3 ] и др.
Аналитические реакции катиона олова (II)
1. Реакция с щелочами: Sn2+ + 2 ОН- - Sn(OH)2 |(белый)
Sn(OH)2 + 2 ОН-= [Sn(OH)4 ]2 '.
2. Реакция с аммиаком: Sn2+ + 2 NH3 -H2 O) — Sn(OH)2 (белый) + 2 NH4CI
Осадок не растворяется в избытке аммиака.
3. Реакция с сульфид - ионами:8Sn2+ + S2 - — SnS . (бурый)
Осадок не растворяется в щелочах, в избытке раствора сульфида натрия..
4. Реакция с солями висмута (III).Олово (II) является хорошим восстановителем:
2 Bi3+ + 3 [Sn(OH)4 ]2 - + 6 ОН- — 2 Bi + 3 [Sn(OH)6 ]2 -
5. Реакция с хлоридом ртути(П): [SnCl4 ]2 -+ 2 HgCI2 -+ Hg2 Cl2 J. + [SnCl6 ]2 -
Выпадает белый осадок каломели Hg2 Cl2 , который постепенно чернеет за счет выделяющейся металлической ртути: [SnCl4 ] -+ Hg2 Cb —> 2 Hg + [SnCl6 ]
Другие реакции олова (II).
Соединения олова (II) при взаимодействии с молибдатом аммония образуют так называемую -молибденовую синь- (раствор окрашивается в синий цвет); с Na2 HPO4 дают белый осадок Sri3(PO4 )2 (растворяется в кислотах и щелочах); при реакции с FeCI3 восстанавливают железо (III) до железа (II), причем в присутствии гексацианоферрата (III) калия K3 [Fe(CN)6 ] раствор сразу же окрашивается в синий цвет вследствие образования турибуллевой сини.